Stärke

|
Einleitung
Stärke allgemein
Stärke ist eine organische Verbindung, die zu den Kohlenhydraten zählt.
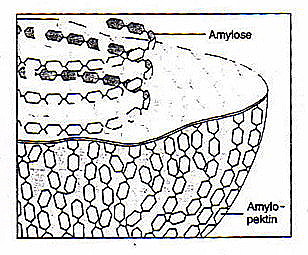
Die Formel lautet (C6H10O5)n. Saccharide werden in Pflanzen in Form von Stärke (Stärkekörnern) gespeichert. Sie besteht zu ca. 20% aus wasserlöslicher Amylose und zu ca. 80% aus wasserunlöslichem Amylopektin.
Durch enzymatischen Abbau kann die Stärke wieder als Energie genutzt werden, ein enzymatischer Abbau findet
auch bei der menschlichen Verdauung statt. Daher ist Stärke einer der wichtigsten Bestandteile in pflanzlichen Zellen.
Stärkegewinnung
Stärke wird aus Getreide, Kartoffeln, Mais und Reis gewonnen.
Amylose
Amylose ist der wasserlösliche, von Amylopektin umhüllter Bestandteil der Stärke.
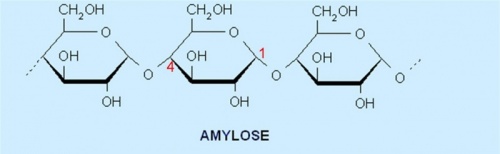
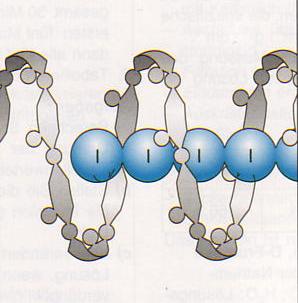
Die Moleküle der Amylose bestehen aus bis zu 10.000 a-Glucose-Einheiten. Die Reste sind α-1,4-glykosidisch miteinander verbunden. In Lösungen liegt die Amylose als Wendel vor, in den sich Polyiodketten einlagern können. Jeder Wendel besteht aus 5-6 Glucoseeinheiten.
Amylose-Nachweis
Bei Zugabe von Iod/Kaliumiodid-Lösung zu einer stärkehaltigen Lösung entsteht ein Iod-Stärke-Komplex mit einer deutlichen Blaufärbung.
Allerdings kann die bei dem Versuch entstandene lodstärke je nach Konzentration auch eine andere Färbung aufweisen (tiefblau, blauviolett bis schwarz). Die Färbung kommt im Licht zustande, weil die Anregungsenergie der Valenzelektronen in der Lösung herabgesetzt wird. Dies ist ein Nachweis für lod und Amylose.
Die blaue Farbe ergibt sich durch den Einschluss des lods in die Wendel. Für die Reaktion sind lodid-Ionen notwendig.
Beim Verdünnen oder Erwärmen löst sich der Einschluss und die Färbung verschwindet.
Amylopektin
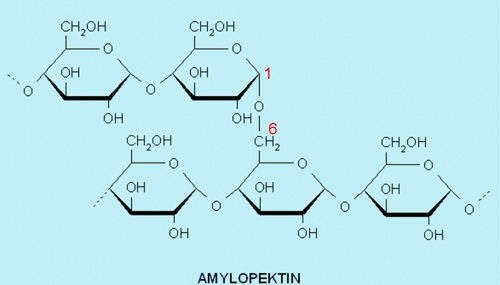
Amylopektin ist durchschnittlich zu 80% in Stärke enthalten. Es besteht genau wie Amylose aus Glucoseeinheiten. Davon gibt es bis zu 1 Millionen. Die Grundstruktur entspricht ebenfalls der Amylose. Allerdings ist Amylopektin verzweigter, da es an jedem 25. Glucoserest zusätzlich eine α-(1,6)-Verbindung hat.
Amylopektin-Nachweis
Versuch: Stärkenachweis mit Iod
Geeignet für die Durchführung in vier Gruppen. Zeitaufwand: 20 bis 25 Minuten.
Gerät
- Becherglas (100 ml)
- Pipette
- Waage
Chemikalien
- Iod-Kaliumiodid-Lösung
- je Gruppe ein bestimmtes Stärkeprodukt wie Weizenmehl, Kartoffelstärke, Maisstärke, Puddingpulver und Kleisterpulver
- destilliertes Wasser
Durchführung
- Gebe 1g eures Stärkeproduktes in ein Becherglas.
- Füge 50 ml destilliertes Wasser hinzu und verrühre die Lösung, bis kein "Klumpen" mehr enthalten sind.
- Füge 5 Tropfen Iod/Kaliumiodid-Lösung hinzu.
Fragestellung
- (vor dem Versuch zu beantworten) Welche Reaktion ist durch das Zufügen von Iod/Kaliumiodid-Lösung zu den verschiedenen Stärkeprodukten?
- Welche Beobachtungen machst du?
- Wie lässt sich die Reaktion erklären?
- Vergleicht eure Reaktionen? Wie lassen sich die Unterschiede erklären?
Die Beispiel-Beobachtung und die Auswertung befinden sich hier.
Verbesserungsvorschläge
- Zinkiodid-Stärkelösung: Während Stärkelösung vor Gebrauch frisch hergestellt werden muss, ist Zinkiodid-Stärkelösung nahezu unbegrenzt haltbar. Herstellung: Man löst 1 g Stärke (lösl.) u. 10 g Zinkchlorid in 50 mL siedendem Wasser. Nach dem Erkalten wird mit einer farblosen Lsg. von 0,5 g Zinkpulver u. 1 g Iod in 5 mL Wasser versetzt, mit Wasser auf 500 mL verdünnt u. filtriert. Alternativ: Statt Zinkchlorid die gleiche Menge Zinkiodid einsetzen, nach Erkalten weitere 1,6g Zinkiodid hinzufügen und mit Wasser auf 500 mL auffüllen.
- Mit Hilfe eines Fotometers lassen sich die Aussagen des Versuches präzisieren. Hierfür wird zunächst eine Konzentrationstabelle angelegt. Diese Tabelle soll die Lichtintensität, die für bestimmte Konzentrationen von Amylose gemessen wurde, darstellen. Die Bestimmung der Konzentration von Amylose, im oben erläuterten Versuch, lässt sich nun durch Messen der Lichtintensität und Vergleichen der erhaltenen Werte mit der zuvor erstellten Tabelle genauer bestimmen.
Tipp: Das Extinktionsmaximum des blauen Iod-Stärke-Komplexes liegt bei 576 nm.
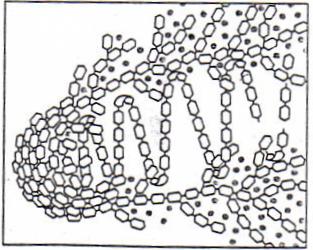
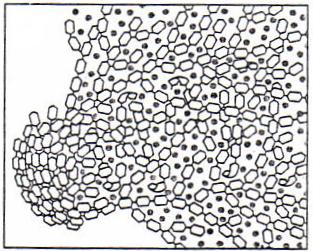
Stärkeverkleisterung
Stärke ist im Allgemeinen in Wasser fast unlöslich. Dieses liegt am Aufbau der Stärke. Der unlösliche Amylopektin umgibt die lösliche Amylose. Beim Erhitzen des Wassers auf 40°C bis 60°C quillt die Stärke jedoch auf, da die äußeren Schichten aufplatzen. Während der Quellung nimmt das Volumen des Stärkekornes stark zu, da es viel Wasser aufnimmt.
Wird das Wasser weiter bis zu einer Temperatur von 55°C bis 87 °C erhitzt, verkleistert die Stärke. Das bedeutet, dass die Struktur sich noch weiter auflöst und das Wasser sich in den entstandenen Zwischenräumen einlagert. Es entsteht eine zähflüssige Lösung. Beim Abkühlung der Lösung verfestigt sich diese.
Dieser Prozess ist ein wichtiger Vorgang für das Herstellen von Gebäcken.
Die Retrogradation ist der umgekehrte Vorgang der Verkleisterung.
Nahrung und Verdauung
Stärke ist in fast jeder pflanzlichen Nahrung enthalten. Eine Ausnahme bilden z. B. Zuckerrohr und Zuckerrüben.
Für die menschliche Ernährung ist Stärke das wichtigste Kohlenhydrat, da es große Mengen von Energie enthält.
Energie
Fragestellung:
- Warum ist Stärke so bedeutend für die menschliche Ernährung?
- Warum ist es gut, wenn ein Marathonläufer vor dem Wettkampf Nudeln ist?
- Energiegewinnung aus KH ist ökonomischer als die aus Fetten, da weniger Sauerstoff benötigt wird
 besondere Bedeutung beim Sportler
besondere Bedeutung beim Sportler - komplexe KH sind besser, da sie einen längeren, kontinuierlichen Blutzuckerspiegel verursachen
- können sowohl im aeroben, als auch im anaeroben Stoffwechsel zur Energiegewinnung dienen
- Nachteil: Glykogen kann nur begrenzt gespeichert werden
- länger andauernde sportliche Betätigungen sind KH wichtig, da Fette nicht so eine hohe Belastungsintensität sichern können
- Breitensportler haben einen erhöhten KH-Bedarf
- Zweifachzucker (Maltose) und Mehrfachzucker sind gleichgut zur Energiebereitstellung geeignet
- größerer Teil jedoch durch Stärke, da die stärkereichen Produkte gleichzeitig Mineralstoffe, Ballaststoffe und Vitamine liefern
Die Verdauung
Bei der Verdauung dient das Enzym Amylase der Amylose als Katalysator und das Enzym Isomaltase dem Amylopektin als Katalysator. Die Enzyme beschleunigen die Hydrolyse von Amylose und Amylopektin.
Diese werden zu Dextrin gespalten. Danach findet der weitere enzymatische Abbau zunächst zu Maltose und dann zu Glucose statt.
Diese dient dem Körper dann als Energie.
Verwendung
Stärke wird sehr vielfältig verwendet. Einige Beispiele sind:
Lebensmittelverarbeitung:
- Herstellung von Cremes, Flammeries, Dekorplatten
- Binden von Suppen und Soßen
- Standfestmachen von Schlagsahne
- Herstellung von Dextrinen und Traubenzucker
- Herstellung mehlhaltigen Nahrungsmitteln (z.B. Brot) und Nährmittel
In der Lebensmittelindustrie wird es häufig unter dem Namen modifizierte Stärke verwendet. Dieses ist Stärke, die chemisch bearbeitet ist.
Durch die chemische Verarbeitung hat die Stärke eine bessere Hitzestabilität, Säurestabilität, Schwerstabilität und ein besseres Gefrier- und Auftauverhalten.
Modifiziere Stärke gilt als Lebensmittelzusatzstoff und muss auf den Verpackungen gekennzeichnet werden.
E 1404 Oxidierte Stärke (oxidativ abgebaute Stärke)
E 1410 Monostärkephosphat
E 1412 Distärkephosphat
E 1413 Phosphatiertes Distärkephosphat
E 1414 Acetyliertes Distärkephosphat
E 1420 Acetylierte Stärke
(siehe auch: E-Nummern)
Weitere Verwendungszwecke:
• Beizen von Baumwolle
• zur Färbung mit Anilinfarben
• zum Leimen von Papier
• zum Verdicken von Farben
• usw.
Historisches
Übungen
Fragen
- Woraus wird Stärke gewonnen?
- Was passiert mit Stärkeprodukten (z.B. einem Stück Brot), wird es in wässriger Lösung gegeben und erhitzt?
- Was findet im Vorgang der Verkleisterung statt?
- Wie heißt der umgekehrte Vorgang der Stärkeverkleisterung und was findet statt?
- Was ist der Unterschied bei der Verdauung von Amylose und Amylopektin?
- Nenne Verwendungsmöglichkeiten für Stärke!
- Welche Eigenschaften sind bei modifizierter Stärke verändert?
Hier findest du die ![]() Antworten.
Antworten.
Zusatzmaterialien
Powerpointpräsentation
Verdauung (Word-Datei)
Aufgabenblatt (Word-Datei)
Sicherheitshinweise
Bei der Verwendung von Stärke beim Experimentieren gilt:
| |
Auf Chemikalien-Gefäßen finden sich codierte Hinweise auf Gefährdungen und entsprechende Vorsorgemaßnahmen beim Umgang mit dieser Chemikalie. Diese sogenannten H- & P-Sätze hängen gemeinsam mit den Arbeitsregeln für Schülerexperimente als Betriebsanweisung im Chemieraum aus und müssen in jedem Fall beachtet werden! |
Experimente
- Hydrolyse von Stärke, in: Chemie heute (Ausgabe 1998), Seite 369, Versuch 5
- Kohlenhydrate: Hydrolyse von Stärke, in: Chemie heute SII, Seite 444, Versuch 5
- Nachweis von Stärke, in: Elemente Chemie 2, Seite 368, Versuch 1
- Gleichgewichtsverschiebung: Iod/Stärke-Reaktion, in: Chemie heute SII, Seite 103, Versuch 3
- Wie viel Gramm Stärke kann man aus einer Kartoffel gewinnen?. In: Friedrich Verlag (Hrsg.): Naturwissenschaften im Unterricht Chemie (Zeitschrift), Heft 175, S. 35 (2020).
- Gewinnung und hydrolytischer Abbau von Stärke (mittels Diastase). In: Friedrich Verlag (Hrsg.): Naturwissenschaften im Unterricht Chemie (Zeitschrift), Heft 175, S. 36 (2020).
| Im Chemiebuch ... | ||
|---|---|---|
| findest Du weitere Informationen zum Thema Stärke: | ||
Chemie FOS-T
auf Seite |
Chemie heute
auf Seite |
Elemente Chemie
auf Seite |
Weblinks
- Stärke als Google-Suchbegriff
- Stärke in der Wikipedia
- Stärke hier in bs-wiki.de mit Google
- Stärke als Youtube-Video
- Sicherheitsdatenblatt für Stärke unseres Lieferanten Bernd Kraft GmbH für Stärkelösung 1% stabilisiert
- Sicherheitsdatenblatt und Produktseite von Stärke (Dextrin aus Kartoffelstärke) unseres Lieferanten Carl Roth
Quellen
- Chemie heute - Sekundarbereich II, Schroedel Verlag, Kapitel 19.4, S. 366/367
- Römpp Lexikon Chemie, Thieme Verlag, Version 2.0, Artikel: Stärke
- Microsoft Encarta Enzyklopädie Professional 2005, Artikel: Stärke, Dextrin
- Grundfragen der Ernährung, Cornelia A. Schlieper, Handwerk und Technik Dr. Felix Büchner - Verlag, Kapitel: 2 Kohlenhydrate, S.22/40/41
- Versuch: http://cc.uni-paderborn.de/studienarbeiten/seidel/allgem_chem/versuche/staerke.html
- Bild vom Weizen: http://www.muehlenchemie.de/deutsch/know-how/index.html
- Bilder vom Stärkekorn: Arbeitsblätter Ernährungslehreunterricht (11. Klasse): "Stärkeverkleisterung"