Acetylsalicylsäure: Unterschied zwischen den Versionen
Dg (Diskussion | Beiträge) |
Dg (Diskussion | Beiträge) (→Quellen) |
||
| Zeile 70: | Zeile 70: | ||
[[Bild:Aspirin.gif]] | [[Bild:Aspirin.gif]] | ||
| − | |||
{{cb|-|408|300}} | {{cb|-|408|300}} | ||
| + | {{www2}} | ||
| + | * http://www.conatex{{c}}mediapool/versuchsanleitungen/VAD_Chemie_Synthese_von_Acetylsalicylsaeure.pdf | ||
* Folienserie des Fonds der Chemischen Industrie, S. 16 | * Folienserie des Fonds der Chemischen Industrie, S. 16 | ||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
[[Kategorie:Chemie]] | [[Kategorie:Chemie]] | ||
[[Kategorie:Chemikalien]] | [[Kategorie:Chemikalien]] | ||
[[Kategorie:Experiment]] | [[Kategorie:Experiment]] | ||
Version vom 30. März 2012, 23:14 Uhr
| Acetylsalicylsäure | ||
|---|---|---|
| vernetzte Artikel | ||
| Arzneimittel | Arzneimittel: Antworten | |
Inhaltsverzeichnis
Allgemein
Acetylsalicylsäure, kurz ASS, ist ein weit verbreiteter schmerzstillender und blutgerinnungs- und entzündungshemmender sowie fiebersenkender Wirkstoff. Namensgebend für den Wirkstoff waren die Weidengewächse (lateinisch Salicaceae), aus denen erstmals diese Substanz gewonnen werden konnte. ASS wurde insbesondere unter dem Markennamen Aspirin® bekannt.
Chemische und physikalische Eigenschaften
Acetylsalicylsäure ist der Trivialname für 2-Acetoxybenzoesäure, wie sie nach den IUPAC-Regularien heißt. Die phenolische Hydroxylgruppe in ortho-Stellung zur Carbonsäuregruppe der o-Hydroxybenzoesäure ist mit Essigsäure verestert. Dadurch hat das Gesamtmolekül einen hydrophilen und einen lipophilen Anteil.
Acetylsalicylsäure liegt als weißes Pulver vor oder bildet flache bis nadelförmige Kristalle mit schwachem Geruch nach Essigsäure. Der pKs-Wert beträgt 3,5. Sie schmilzt bei einer Temperatur von 135 °C, ihr Zersetzungspunkt liegt bei ca. 140 °C. Acetylsalicylsäure ist gut löslich in Ethanol, Alkalilauge, aber schlecht löslich in Benzol oder kaltem Wasser (3,3 g·l−1 bei 20 °C). Die Wasserlöslichkeit steigt erheblich beim Erwärmen. Die Dichte von Acetylsalicylsäure beträgt 1,35 g·cm−3.
Fehlindikationen
Als Schmerzmittel zur Unterdrückung von Wundschmerz wie z.B. nach chirurgischen Eingriffen oder Verletzungen ist Acetylsalicylsäure ungeeignet, da die gerinnungshemmende Wirkung bis etwa 7 Tage nach der letzten Einnahme anhält und damit Blutungen begünstigt. Wegen der irreversiblen Hemmung der Cyclooxygenase in den Thrombozyten ist auch eine Gabe eines Gegenmittels zur sofortigen Aufhebung der Gerinnungshemmung nicht möglich. Es muss vielmehr abgewartet werden, bis neue, funktionsfähige Thrombozyten vom Körper gebildet werden. Auf diese Weise kann eingenommene Acetylsalicylsäure eine dringende medizinische Operation (oder ihren Termin) vereiteln, denn mangelnde Gerinnung führt zu Komplikationen wie zu großem Blutverlust. Auf jeden Fall müssen die behandelnden Ärzte über die Acetylsalicylsäure-Einnahme informiert werden.
Synthese von Acetylsalicylsäure
Geräte
- Bunsenbrenner
- Sicherheitsbrille
- Waage
- Einwegspritze
- Erlenmeyerkolben (100 ml)
- Becherglas (250 ml)
- Büchner-Trichter mit Saugflasche
- Schale
- Spatel
- Thermometer
Chemikalien
- Salicylsäure (2g)
- Essigsäureanhydrid (5mL)
- Schwefelsäure (5 Tropfen)
Sicherheit
| Stoffe | R-Sätze und S-Sätze | Schädlichkeit |
|---|---|---|
| Salicylsäure | R: 22-41 S: 22-24-26-39 | Gesundheitsschädlich |
| Essigsäureanhydrid | R: 10-20/22-34 S: (1/2)-26-36/37/39-45 | ätzend |
| Schwefelsäure | R: 35 S: (1/2)-26-30-45 | ätzend |
Durchführung
- Vermische im Erlenmeyerkolben 2g Salicylsäure mit 5 mL Essigsäureanhydrid, füge fünf Tropfen Schwefelsäure zu und erhitze das Gemisch zwei Minuten im siedenden Wasserbad.
- Hydrolysiere überschüssiges Anhydrid in der heißen Lösung mit einigen Tropfen Wasser. Gieße das Gemisch anschließend in 100 ml Wasser.
- Sauge den Niederschlag ab und wasche mehrmals mit kaltem Wasser. Trockne das Produkt über Nacht bei 90°C.
Beobachtung
Während des Versuchs wird die Salicylsäure mit dem Essigsäureanhydrid synthetisiert. Nach dem zweiminütigen Erhitzen der beiden Stoffe werden sie in ein Wasserbad gegeben und es bildet sich eine weiße Masse heraus.
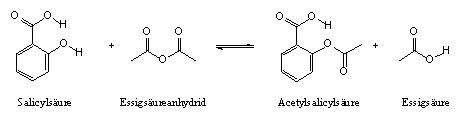
Reaktionsgleichung
| Im Chemiebuch ... | ||
|---|---|---|
| findest Du weitere Informationen zum Thema Acetylsalicylsäure: | ||
Chemie FOS-T
auf Seite |
Chemie heute
auf Seite |
Elemente Chemie
auf Seite |
Experimente und weitere Informationen zum Thema
- {{{1}}} als Google-Suchbegriff
- {{{1}}} in der Wikipedia
- {{{1}}} hier in bs-wiki.de mit Google
- {{{1}}} als Youtube-Video
- http://www.conatex.com/mediapool/versuchsanleitungen/VAD_Chemie_Synthese_von_Acetylsalicylsaeure.pdf
- Folienserie des Fonds der Chemischen Industrie, S. 16