Molare Masse: Unterschied zwischen den Versionen
Dg (Diskussion | Beiträge) |
Dg (Diskussion | Beiträge) |
||
| (28 dazwischenliegende Versionen desselben Benutzers werden nicht angezeigt) | |||
| Zeile 1: | Zeile 1: | ||
{{navi|Stöchiometrie|Atommasse}} | {{navi|Stöchiometrie|Atommasse}} | ||
| − | Die <b>molare Masse</b> | + | Die <b>molare Masse</b> ''M'' (Einheit: g/mol) ist eine für [[Stöchiometrie|stöchiometrische Berechnungen]] benötigte stoffspezifische [[Größe]], die sich |
# über die [[Atommasse]]n aus der [[Summenformel]] einer chemischen Substanz ableiten lässt | # über die [[Atommasse]]n aus der [[Summenformel]] einer chemischen Substanz ableiten lässt | ||
| − | # aus dem Verhältnis einer Masse m zur [[Stoffmenge]] n errechnen lässt: M = m / n | + | # aus dem Verhältnis einer Masse ''m'' zur [[Stoffmenge]] ''n'' errechnen lässt:<br /><br />{{Formel|1=''[[molare Masse|M]] = [[Masse|m]] / [[Stoffmenge|n]]''}}<br /><br /> |
# [[Experiment|experimentell]] bestimmen lässt (s.u.) | # [[Experiment|experimentell]] bestimmen lässt (s.u.) | ||
| − | == | + | == Experimentelle Ermittlung der molaren Masse eines Gases == |
| − | + | Von Janne-Claas K.; WG11B: | |
| − | |||
| − | Von Janne-Claas | ||
| + | Geräte: [[Gaswägekugel]] (1 L), [[Messzylinder]] (100 mL), [[Waage]], Schlauch | ||
| − | geg: M(C<sub>n</sub>H<sub>2n+2</sub>) = 43,2g/mol | + | Chemikalien: Nachfüllpatrone mit Feuerzeuggas (F+) |
| + | |||
| + | Durchführung: | ||
| + | |||
| + | # Verschließe die Gaswägekugel und bestimme die Masse der mit Luft gefüllten Kugel. | ||
| + | # Lasse das Feuerzeuggas so lange einströmen, bis alle Luft verdrängt ist. | ||
| + | # Verschließe die Kugel wieder, wiege erneut und berechne die Massendifferenz. | ||
| + | # Befülle die Gaswägekugel mit Wasser und bestimme mit Messzylinder das genaue Füllvolumen. | ||
| + | |||
| + | Auswertungsbeispiel: Für ein gasförmiges [[Alkan]] ergab sich eine Massendifferenz von +0,6 g. Ein Liter [[Luft]] hat bei Raumtemperatur die Masse 1,2 g. Ein Liter des Gases hat daher die Masse 1,8 g. Bei Raumtemperatur beträgt das [[molares Volumen|molare Volumen]] etwa 24 L/mol. | ||
| + | |||
| + | ''n''(Gas) = ''V''(Gas)/''V''m = 1 L{{*}}mol / 24 L = 0,0417 mol | ||
| + | |||
| + | ''M''(Gas) = ''m''(Gas)/''n''(Gas) = 1,8 g / 0,0417 mol = 43,2 g/mol | ||
| + | |||
| + | Aufgabe: Um welches Alkan könnte es sich handeln? | ||
| + | |||
| + | geg: ''M''(C<sub>n</sub>H<sub>2n+2</sub>) = 43,2g/mol | ||
ges: n (als Index der Summenformel) | ges: n (als Index der Summenformel) | ||
| Zeile 17: | Zeile 33: | ||
{| {{Tabelle}} align="center" | {| {{Tabelle}} align="center" | ||
! n | ! n | ||
| − | ! M in g/mol | + | ! ''M'' in g/mol |
! Alkan | ! Alkan | ||
|- | |- | ||
| Zeile 33: | Zeile 49: | ||
|} | |} | ||
| − | Antwort: Es muss sich bei dem Alkan um Propan handeln (C<sub>3</sub>H<sub>8</sub>), dies kann man ebenfalls mit der aus den molaren Massen abgeleiteten Formel errechnen: n = (M-2)/14 | + | Antwort: Es muss sich bei dem Alkan um Propan handeln (C<sub>3</sub>H<sub>8</sub>), dies kann man ebenfalls mit der aus den molaren Massen abgeleiteten Formel errechnen: n = (''M''-2)/14 |
| + | == Übungen == | ||
| + | Zusatzaufgabe Nr. 1: | ||
| − | |||
a) Berechne die Dichte von [[Kohlenstoffmonooxid]] mit Hilfe der molaren Masse des Stoffes. | a) Berechne die Dichte von [[Kohlenstoffmonooxid]] mit Hilfe der molaren Masse des Stoffes. | ||
| − | |||
| − | |||
| − | |||
| + | geg: ''M''(CO) = 28g/mol; ''V''mo = 22,4 L/mol | ||
| − | + | Ges: ρ(CO) (ρ = Dichte) | |
| + | ρ(CO) = ''M''(CO){{*}}''V''mo = (28g{{*}}mol)/(22,4mol{{*}}L) = 1,25 g/L | ||
Antwort: Kohlenstoffmonooxid hat eine Dichte von 1,25g/L. | Antwort: Kohlenstoffmonooxid hat eine Dichte von 1,25g/L. | ||
| + | |||
b) Vergleiche die Dichte von Kohlenstoffmonooxid mit der Dichte von Stickstoff. | b) Vergleiche die Dichte von Kohlenstoffmonooxid mit der Dichte von Stickstoff. | ||
| − | + | ρ(CO) = 1,25g/L = ρ(N<sub>2</sub>) | |
Antwort: Da die molare Masse gleich ist, ist auch die Dichte gleich. | Antwort: Da die molare Masse gleich ist, ist auch die Dichte gleich. | ||
| Zeile 56: | Zeile 73: | ||
Zusatzaufgabe Nr. 2: | Zusatzaufgabe Nr. 2: | ||
| − | Für eine organische Verbindung wurde die Verhältnisformel C<sub>1</sub>H<sub>1</sub> ermittelt. 800mg der Substanz wurden verdampft. Bei 95°C ergab sich ein Volumen von 300mL. Der Druck | + | Für eine [[organische Verbindung]] wurde die Verhältnisformel C<sub>1</sub>H<sub>1</sub> ermittelt. 800mg der Substanz wurden verdampft. Bei 95°C ergab sich ein Volumen von 300mL. Der Druck war 1013 hPa. Berechne die molare Masse und ermittel die [[Molekülformel]]. |
| − | geg: C<sub>1</sub>H<sub>1</sub>; T<sub>0</sub>=95°C = 368,15K; V=300mL=0,3L; p= | + | geg: C<sub>1</sub>H<sub>1</sub>; ''T''<sub>0</sub> = 95°C = 368,15K; ''V'' = 300mL = 0,3L; ''p'' = 1.013hPa; m = 0,8g; [[allgemeine Gaskonstante|R]] = 83,144 hPa{{*}}L{{*}}mol<sup>-1</sup>{{*}}K<sup>-1</sup> |
| − | |||
| − | M(C<sub> | + | ges: ''M''(C<sub>n</sub>H<sub>n</sub>) |
| − | + | ''M''(C<sub>1</sub>H<sub>1</sub>) = 13g/mol | |
| + | ''M'' = 78g/mol | ||
| − | + | Antwort: Die molare Masse beträgt 78g/mol und die Summenformel ist C<sub>6</sub>H<sub>6</sub> ([[Benzol]]). | |
| − | |||
Von den möglichen Strukturformeln ergibt sich nach Kekulé ein Sechsring: | Von den möglichen Strukturformeln ergibt sich nach Kekulé ein Sechsring: | ||
| + | [[Bild:Benzol.png]] | ||
| − | {{cb|-|223}} | + | {{cb|98|223|508}} |
| − | [[Kategorie:Chemie]][[Kategorie:Methoden]] | + | {{www2}} |
| + | {{Ex-ch|223|1-2|Ermittlung der molaren Masse}} | ||
| + | {{Ex-ec|72|1-2|Ermittlung der molaren Masse}} | ||
| + | {{Ex-ch09|{{fb|262}}|1|Ermittlung der molaren Masse|Molare Masse}} | ||
| + | {{Ex-ch09|{{fb|262}}|2|Ermittlung der molaren Masse|Molare Masse von Feuerzeuggas}} | ||
| + | {{Ex-ch09|{{fb|262}}|3|Ermittlung der molaren Masse|Molare Masse durch Gefriertemperaturerniedrigung}} | ||
| + | * [http://pse.merck.de/labtools/molar_mass.html Molmassenrechner Fa. Merck] | ||
| + | [[Kategorie:Chemie]][[Kategorie:Methoden]][[Kategorie:Experiment]][[Kategorie:Stoffeigenschaft]] | ||
| + | [[Kategorie:Physikalische Größe]] | ||
Aktuelle Version vom 14. September 2017, 19:26 Uhr
| Molare Masse | ||
|---|---|---|
| vernetzte Artikel | ||
| Stöchiometrie | Atommasse | |
Die molare Masse M (Einheit: g/mol) ist eine für stöchiometrische Berechnungen benötigte stoffspezifische Größe, die sich
- über die Atommassen aus der Summenformel einer chemischen Substanz ableiten lässt
- aus dem Verhältnis einer Masse m zur Stoffmenge n errechnen lässt:
M = m / n - experimentell bestimmen lässt (s.u.)
Experimentelle Ermittlung der molaren Masse eines Gases
Von Janne-Claas K.; WG11B:
Geräte: Gaswägekugel (1 L), Messzylinder (100 mL), Waage, Schlauch
Chemikalien: Nachfüllpatrone mit Feuerzeuggas (F+)
Durchführung:
- Verschließe die Gaswägekugel und bestimme die Masse der mit Luft gefüllten Kugel.
- Lasse das Feuerzeuggas so lange einströmen, bis alle Luft verdrängt ist.
- Verschließe die Kugel wieder, wiege erneut und berechne die Massendifferenz.
- Befülle die Gaswägekugel mit Wasser und bestimme mit Messzylinder das genaue Füllvolumen.
Auswertungsbeispiel: Für ein gasförmiges Alkan ergab sich eine Massendifferenz von +0,6 g. Ein Liter Luft hat bei Raumtemperatur die Masse 1,2 g. Ein Liter des Gases hat daher die Masse 1,8 g. Bei Raumtemperatur beträgt das molare Volumen etwa 24 L/mol.
n(Gas) = V(Gas)/Vm = 1 L · mol / 24 L = 0,0417 mol
M(Gas) = m(Gas)/n(Gas) = 1,8 g / 0,0417 mol = 43,2 g/mol
Aufgabe: Um welches Alkan könnte es sich handeln?
geg: M(CnH2n+2) = 43,2g/mol
ges: n (als Index der Summenformel)
| n | M in g/mol | Alkan |
|---|---|---|
| 1 | 16 | CH4 |
| 2 | 30 | C2H6 |
| 3 | 44 | C3H8 |
Antwort: Es muss sich bei dem Alkan um Propan handeln (C3H8), dies kann man ebenfalls mit der aus den molaren Massen abgeleiteten Formel errechnen: n = (M-2)/14
Übungen
Zusatzaufgabe Nr. 1:
a) Berechne die Dichte von Kohlenstoffmonooxid mit Hilfe der molaren Masse des Stoffes.
geg: M(CO) = 28g/mol; Vmo = 22,4 L/mol
Ges: ρ(CO) (ρ = Dichte)
ρ(CO) = M(CO) · Vmo = (28g · mol)/(22,4mol · L) = 1,25 g/L
Antwort: Kohlenstoffmonooxid hat eine Dichte von 1,25g/L.
b) Vergleiche die Dichte von Kohlenstoffmonooxid mit der Dichte von Stickstoff.
ρ(CO) = 1,25g/L = ρ(N2)
Antwort: Da die molare Masse gleich ist, ist auch die Dichte gleich.
Zusatzaufgabe Nr. 2:
Für eine organische Verbindung wurde die Verhältnisformel C1H1 ermittelt. 800mg der Substanz wurden verdampft. Bei 95°C ergab sich ein Volumen von 300mL. Der Druck war 1013 hPa. Berechne die molare Masse und ermittel die Molekülformel.
geg: C1H1; T0 = 95°C = 368,15K; V = 300mL = 0,3L; p = 1.013hPa; m = 0,8g; R = 83,144 hPa · L · mol-1 · K-1
ges: M(CnHn)
M(C1H1) = 13g/mol
M = 78g/mol
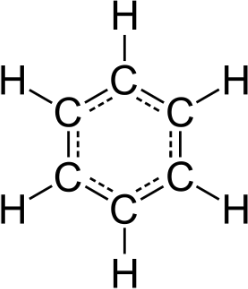
Antwort: Die molare Masse beträgt 78g/mol und die Summenformel ist C6H6 (Benzol).
Von den möglichen Strukturformeln ergibt sich nach Kekulé ein Sechsring:
| Im Chemiebuch ... | ||
|---|---|---|
| findest Du weitere Informationen zum Thema Molare Masse: | ||
Chemie FOS-T
auf Seite |
Chemie heute
auf Seite |
Elemente Chemie
auf Seite |
Experimente und weitere Informationen zum Thema
- {{{1}}} als Google-Suchbegriff
- {{{1}}} in der Wikipedia
- {{{1}}} hier in bs-wiki.de mit Google
- {{{1}}} als Youtube-Video
- Ermittlung der molaren Masse, in: Chemie heute (Ausgabe 1998), Seite 223, Versuch 1-2
- Ermittlung der molaren Masse, in: Elemente Chemie 2, Seite 72, Versuch 1-2
- Ermittlung der molaren Masse: Molare Masse, in: Chemie heute SII, Seite 262, Versuch 1
- Ermittlung der molaren Masse: Molare Masse von Feuerzeuggas, in: Chemie heute SII, Seite 262, Versuch 2
- Ermittlung der molaren Masse: Molare Masse durch Gefriertemperaturerniedrigung, in: Chemie heute SII, Seite 262, Versuch 3
- Molmassenrechner Fa. Merck