Natriumacetat: Unterschied zwischen den Versionen
Aus BS-Wiki: Wissen teilen
Dg (Diskussion | Beiträge) |
Dg (Diskussion | Beiträge) |
||
| Zeile 4: | Zeile 4: | ||
[[molare Masse|M]] = 82 g/mol, [[Dichte]] = 1,45 g/cm<sup>3</sup>, [[Schmelzpunkt]] = 58 °C. | [[molare Masse|M]] = 82 g/mol, [[Dichte]] = 1,45 g/cm<sup>3</sup>, [[Schmelzpunkt]] = 58 °C. | ||
| − | Als Tri[[hydrat]] CH<sub>3</sub>COONa{{*}}3H<sub>2</sub>O farb- u. geruchlose, bitter-salzig schmeckende Kristalle, spaltet bei 120 °C Kristallwasser ab (Schmp. 324 °C), leicht lösl. in Wasser, mäßig lösl. in Alkohol. In wäss. Lsg. ist das Salz prakt. vollständig dissoziiert mit schwach alkal. Reaktion. | + | Als Tri[[hydrat]] CH<sub>3</sub>COONa{{*}}3H<sub>2</sub>O farb- u. geruchlose, bitter-salzig schmeckende Kristalle, spaltet bei 120 °C [[Kristallwasser]] ab (Schmp. 324 °C), leicht lösl. in Wasser, mäßig lösl. in Alkohol. In wäss. Lsg. ist das Salz prakt. vollständig dissoziiert mit schwach alkal. Reaktion. |
== Verwendung == | == Verwendung == | ||
Version vom 18. März 2012, 17:53 Uhr
| Natriumacetat | ||
|---|---|---|
| vernetzte Artikel | ||
| Salz | Acetat | |
Natriumacetat (CH3COONa) ist das Na-Salze der Essigsäure, Acetat-Ion: CH3COO¯.
M = 82 g/mol, Dichte = 1,45 g/cm3, Schmelzpunkt = 58 °C.
Als Trihydrat CH3COONa · 3H2O farb- u. geruchlose, bitter-salzig schmeckende Kristalle, spaltet bei 120 °C Kristallwasser ab (Schmp. 324 °C), leicht lösl. in Wasser, mäßig lösl. in Alkohol. In wäss. Lsg. ist das Salz prakt. vollständig dissoziiert mit schwach alkal. Reaktion.
Verwendung
- Puffersubstanz in essigsauren Lsg.: Enthält eine Lösung gleiche Stoffmengen an Essigsäure und Natriumacetat, so erhält man eine Pufferlösung mit dem pH-Wert 4,65. Beispiel:
Bei der Neutralisation von Essigsäure mit Natronlauge entsteht Natriumacetat und Wasser: CH3COOH + NaOH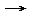 CH3COONa + H2O
CH3COONa + H2O - Füllung von Wärmespeichern (hohe Schmelzenthalpie)
- Lebensmittelzusatzstoff (Konservierungsstoff Natriumdiacetat E 262).
Sicherheitshinweise
Bei der Verwendung von Natriumacetat beim Experimentieren gilt:
| |
Auf Chemikalien-Gefäßen finden sich codierte Hinweise auf Gefährdungen und entsprechende Vorsorgemaßnahmen beim Umgang mit dieser Chemikalie. Diese sogenannten H- & P-Sätze hängen gemeinsam mit den Arbeitsregeln für Schülerexperimente als Betriebsanweisung im Chemieraum aus und müssen in jedem Fall beachtet werden! |
