Ozon: Unterschied zwischen den Versionen
Dg (Diskussion | Beiträge) |
Dg (Diskussion | Beiträge) |
||
| Zeile 1: | Zeile 1: | ||
{{navi|Atmosphäre|Luft}} | {{navi|Atmosphäre|Luft}} | ||
| + | |||
| + | == Chemische Grundlagen == | ||
[[Bild:Ozon2.jpg|thumb|200px|'''O<sub>2</sub> → 2 O∙'''<br />Bild 1: Aufspaltung von Sauerstoffmolekülen zu Radikalen]] | [[Bild:Ozon2.jpg|thumb|200px|'''O<sub>2</sub> → 2 O∙'''<br />Bild 1: Aufspaltung von Sauerstoffmolekülen zu Radikalen]] | ||
| − | |||
| − | |||
Ozon (griechisch ''ozein'': „das Duftende“) ist bei Zimmertemperatur und unter normalem Luftdruck ein blassblaues, giftiges Gas mit durchdringendem Geruch. | Ozon (griechisch ''ozein'': „das Duftende“) ist bei Zimmertemperatur und unter normalem Luftdruck ein blassblaues, giftiges Gas mit durchdringendem Geruch. | ||
Es ist eine besondere Form von [[Sauerstoff]], seine Moleküle sind im Gegensatz zu biatomaren Sauerstoff (O<sub>2</sub>) '''aus drei Sauerstoffatomen aufgebaut''', daher die Formel '''O<sub>3</sub>'''. | Es ist eine besondere Form von [[Sauerstoff]], seine Moleküle sind im Gegensatz zu biatomaren Sauerstoff (O<sub>2</sub>) '''aus drei Sauerstoffatomen aufgebaut''', daher die Formel '''O<sub>3</sub>'''. | ||
Version vom 18. März 2010, 16:54 Uhr
Inhaltsverzeichnis
Chemische Grundlagen
Ozon (griechisch ozein: „das Duftende“) ist bei Zimmertemperatur und unter normalem Luftdruck ein blassblaues, giftiges Gas mit durchdringendem Geruch. Es ist eine besondere Form von Sauerstoff, seine Moleküle sind im Gegensatz zu biatomaren Sauerstoff (O2) aus drei Sauerstoffatomen aufgebaut, daher die Formel O3.
Entstehung
- Bild 1: Unter der Einwirkung des UV-Lichts der Sonne, aber auch bei elektrischen Entladungen, z.B. bei Gewittern, wird das "normale", also biatomare Sauerstoffmolekül aufgespalten, dabei entstehen zwei einzelne Sauerstoffatome (Sauerstoffradikale, O∙).
- Bild 2: Die einzelnen Sauerstoffatome sind extrem reaktionsfreudig und verbinden sich mit einem verbleibenden Sauerstoffmolekül zum O3-Molekül Ozon.
Physiologische Wirkung
Folgen einer zu hohen Ozondosis:
- Kopfschmerzen und Mattigkeit
- Reizwirkungen auf die Augen (Bindehautentzündung)
- Atembeschwerden bei Säuglingen und Kleinkindern, bei Patienten mit Asthma bronchial, Chronische Bronchitis und Herz-Kreislauf-Beschwerden
Technischer Nutzen
- Ozon wird zum Entfernen von Substanzen und Pharmazeutika genutzt, die im Abwasser und sogar im Trinkwasser vorkommen.
- Zusammen mit UV-Licht wird das Ozon auch zur Trinkwasseraufbereitung verwendet, da Ozon keimtötend wirkt.
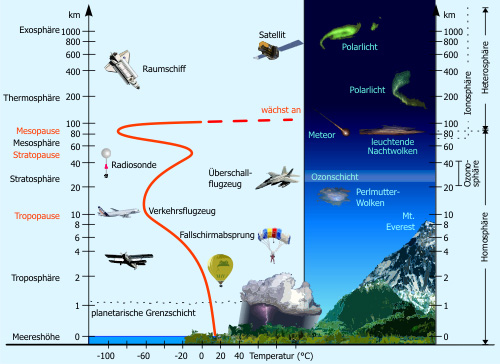
Ozon in der Atmosphäre
Ozon kommt in verschiedenen Schichten der Atmosphäre als Spurengas vor. Wesentlich für die kontroverse Diskussion um atmosphärisches Ozon ist die unterschiedliche Bedeutung des Ozons in Bodennähe (Troposphäre) und in höheren Schichten bis zu 50 km (Stratosphäre).
Troposphäre (bodennahes Ozon)
Das Ozon in Bodennähe ragt bis zu 15 km in die Atmosphäre. In dieser Ebene wirkt das Ozon als Reizgas. Ein Teil dieser Reaktion sind Stickoxide und diese wiederum entstehen bei der Verbrennung von fossilen Brennstoffen, z.B. im Straßen- und Flugverkehr sowie bei Verbrennungsprozessen in der Industrie. Der andere Teil der Reaktion sind flüchtige organische Verbindungen und diese beiden Komponenten wirken bei intensiver Sonneneinstrahlung als Reizgas. Die Wirkung des Ozons in Bodennähe ist für Menschen, Pflanzen und Tiere gesundheitsschädigend. Wenn die Ozonkonzentration über dem Grenzwert von 120 μg/m³ liegt, ist dies schädlich für die Gesundheit. Die Reaktion der Menschen auf die hohen Ozonwerte ist unter dem Punkt Physiologische Wirkung nachzulesen.
Die Ozon-Konzentration in Reinluftgebieten ist im Sommer teilweise höher als in den Städten. Durch die vielen Autoabgase in den Städten, ist die NO-Konzentration sehr hoch. Dieses Stickoxid wirkt der Ozonbildung entgegen.
NO2 + UV-Strahlung → NO∙ + O∙ (Reaktion 1)
O∙ + O2 → O3 (Reaktion 2)
Abbau durch NO
O3 + NO∙ → NO2 + O2 (Reaktion 3)
Je stärker die Sonne scheint, desto mehr Ozon und umso weniger NO2 ist vorhanden. NO2 wird durch die UV-Strahlung gespalten.
In der Atmosphäre befinden sich auch Kohlenwasserstoffe, die sowohl von Menschen als auch von Vegetationen verursacht werden. HC werden von OH-Radikalen oxidiert und zu Peroxid-Radikalen R-O-O · . Die Peroxid-Radikale oxidieren NO zu NO2, ohne dass dabei O3 verbraucht wird.
R-O-O∙ + NO → R-O∙ + NO2 (Reaktion 4)
Der Kreislauf schließt sich, wenn die Reaktionen 1 und 2 wieder stattfinden.
Stratosphäre (atmosphärisches Ozon)
Die von 15-50 km über der Erde reichende Gasschicht, die sogenannte Stratosphäre, ist eine Gasschicht mit besonders viel Ozon. Dieses Ozon ist wiederum besonders wichtig für die Erde, da sie wie ein Filter wirkt und die harten ultravioletten Sonnenstrahlen absorbiert und sie dann in Wärme umwandelt. Hierbei wird eun erheblicher Anteil des UV-Lichtes daran gehindert, bis zur Erdoberfläche durchzudringen. Somit schützt sie also Menschen, Tiere und Pflanzen. Die übrig gebliebene UV-Strahlung, die die Oberfläche erreicht, kann jedoch, bei entsprechender Dosis zu Sonnenbrand bishin zum Hautkrebs führen.
In der Stratosphäre herrscht normalerweise ein Gleichgewicht zwischen dem natürlichen Ab- und Aufbau des Ozons. Dieses Gleichgewicht wird jedoch von Fluor-Chlor-Kohlenwasserstoffen gestört. Durch diesen Ablauf wird die Ozonschicht geschädigt und somit kann man von einer Entstehung des Ozonlochs reden.
Ozonloch
Beim natürlichen Auf- und Abbau des Ozons entsteht in der Stratosphäre ein Gleichgewicht. Dieses Gleichgewicht wird von Fluorchlorkohlenwasserstoffen gestört. Sie tragen dazu bei, dass mehr Ozon zersetzt wird als das sich Neues bilden kann. Durch Luftbewegungen in der Atmosphäre verteilen sich die FCKW rund um die Erde. Da ihre Moleküle sehr stabil gegen äußere Einflüsse sind, verändern sie sich beim Kontakt mit anderen Molekülen nicht. In der Stratosphäre werden jedoch durch die intensive UV-Strahlung aus den FCKW reaktionsfähige Chlorradikale abgespalten. Diese wiederum greifen die Ozonmoleküle an und bewirken deren Umwandlung in Sauerstoffmoleküle. Dabei entsteht außerdem das radikale Chlormonooxid.
Durch die Ausdünnung der Ozonschicht gelangen vor allem UV-B-Strahlungen auf die Erde. Diese Strahlen stellen für alle Lebewesen eine große Bedrohung dar.
- sie verursacht Sonnenbrände und Hautkrebs
- sie schädigt die Augen, fördert den grauen Star und kann bis zur Erblindung führen
- sie schwächt das Immunsystem
- sie schädigt die Erbsubstanz, es wäre denkbar, dass die Menschen unfruchtbar werden, dass die Krebsrate ansteigt oder dass vermehrt Missbildungen vorkommen.
Zusammenfassung
Das Ozon in der Stratosphäre ist besonders wichtig für uns, da es die UV-Strahlung absorbiert und somit die Menschen, Tiere und Pflanzen auf der Erde schützt. Dagegen ist das Ozon in der Troposphäre, wenn es in zu hohen Konzentrationen vorkommt, gesundheitsgefährdend.
- Ozon hat eine nützliche Wirkung in der Stratosphäre, aber eine schädliche Wirkung in Bodennähe.
Lösungsansätze
- Verminderung verkehrsbedingte Emissionen von Stickoxiden, z.B. durch Fahrverbot an Sonntagen und Tempolimit auf den Autobahnen
- Bei der Stromerzeugung auf Solarenergie umstellen
- Verminderung der FCKW-Emissionen, z.B. durch Einsatz vonn FCKW-freien Kühlschränken
Fragebogen
Versuche
Sicherheitshinweise
Bei der Verwendung von Ozon beim Experimentieren gilt:
| |
Auf Chemikalien-Gefäßen finden sich codierte Hinweise auf Gefährdungen und entsprechende Vorsorgemaßnahmen beim Umgang mit dieser Chemikalie. Diese sogenannten H- & P-Sätze hängen gemeinsam mit den Arbeitsregeln für Schülerexperimente als Betriebsanweisung im Chemieraum aus und müssen in jedem Fall beachtet werden! |
| Im Chemiebuch ... | ||
|---|---|---|
| findest Du weitere Informationen zum Thema Ozon: | ||
Chemie FOS-T
auf Seite |
Chemie heute
auf Seite |
Elemente Chemie
auf Seite |
Weblinks
- Ozon als Google-Suchbegriff
- Ozon in der Wikipedia
- Ozon hier in bs-wiki.de mit Google
- Ozon als Youtube-Video
- Prof. Blumes Bildungsserver für Chemie
- Luftüberwachung in Niedersachsen mit aktuellen Ozon-Messwerten
- Foliensatz
- Ozon und Ozonloch
- Ozonschicht
- Bodennahes Ozon
- Bodennahes Ozon 2
- Was ist Ozon?
- Stratosphäre
- Stratosphäre 2
- "Ozonloch" in der Stratosphäre?