|
|
| (49 dazwischenliegende Versionen von 3 Benutzern werden nicht angezeigt) |
| Zeile 1: |
Zeile 1: |
| − | [[Bild:lala.jpg]] | + | {{navi|Proteine|Aminosäuren}} |
| − | #[[Benutzer:Johannes|Johannes]]
| + | {| |
| − | #[[Benutzer:Mille|Mille]]
| + | | __TOC__ || |
| | + | | [[Bild:lala.jpg]] |
| | + | |} |
| | | | |
| − | [[Kategorie:Ernährungslehre]]
| + | ==Peptide== |
| − | [[Kategorie:Chemie]][[Kategorie:Chemikalien]]
| |
| | | | |
| − | Gliederung
| + | ''griech.: peptos = verdaulich'' |
| | | | |
| − | #Proteine
| + | Bez. für durch Peptid-Bindungen säureamid-artig verknüpfte [[Dehydratisierung|Kondensation]]sprodukte von [[Aminosäuren]]. |
| − | #Aminosäuren
| |
| − | #Peptide
| |
| − | #Entstehung von Peptidbindungen
| |
| | | | |
| − | ==Proteine== | + | ==Peptidbinung== |
| − | | |
| − | (Eiweiße, Eiweißstoffe, Eiweißkörper). Auf Berzelius zurückgehende u. seit Mulder (1838) gebräuchliche u. von griech.: proteuein = „der Erste sein“ abgeleitete Sammelbez. für natürlich vorkommende Copolymere, die sich in der Regel aus 20 verschiedenen a-Aminosäuren (im folgenden: AS) als Monomeren zusammensetzen. Von den nahe verwandten Polypeptiden werden sie aufgrund ihrer mol. Größe unterschieden, wenn auch nicht immer streng abgegrenzt: Ab etwa 100 Monomer-Einheiten (AS-Resten) spricht man meist von Proteinen. Es ergeben sich MR von 10 000 bis mehrere Millionen.
| |
| | | | |
| − | Die Aufeinanderfolge der einzelnen Bausteine (AS-Sequenz, Primärstruktur) unterliegt im allg. keinen offensichtlichen Gesetzmäßigkeiten, so daß potentiell jede Kombination möglich ist. Gäbe es von jedem möglichen Protein-Mol. nur ein Exemplar u. würden nur Mol.-Größen entsprechend 150 AS-Einheiten betrachtet, so ergäbe sich bei 20 verschiedenen AS die unvorstellbar große Zahl von 20150 (eine Zahl mit 195 Stellen) unterschiedlicher Mol., die unser Weltall etwa 1090-mal auffüllen könnten. Die Auswahl aus dieser Fülle treffen die Lebewesen nach Maßgabe der genet. Information (s. bei Biosynth.). Man schätzt, daß in unserem Lebensraum ca. 1011 verschiedene P. vorkommen; ein Höherer Organismus soll ca. 105–106 verschiedene P. enthalten.
| + | Eine Peptidbindung (-NH-CO-) ist eine Bindung zwischen der [[Carboxylgruppe]] einer und der [[Aminogruppe]] einer zweiten Aminosäure. |
| | | | |
| − | Man teilt die P. nach Gestalt u. Verhalten gegen Wasser u. Salze ein in: globuläre od. Sphäroproteine, z. B. Albumine, Globuline, Gluteline, Histone, Prolamine, Protamine, sowie: Skleroproteine od. fibrilläre, Gerüst- od. Faser-Proteine (Gerüst-Eiweiß), z. B. Keratine, Fibroin, Elastin, Collagen. Nach der Zusammensetzung trifft man die Einteilung in einfache P., deren Hydrolyse nur AS gibt, u. zusammengesetzte P. (konjugierte Proteine, veraltet: Proteide), die außer AS für die spezif. Eigenschaften essentielle Nichtproteinkomponenten – die prosthetischen Gruppen (in Klammern; ggf. mit Beisp.) – enthalten: Nucleoproteine (Nucleinsäuren; Chromatin), Glykoproteine (Kohlenhydrate; Lectine, Immunglobuline, Blutgruppensubstanzen), Lipoproteine (Lipide), Phosphoproteine (Phosphorsäure; Casein, Vitelline), Chromoproteine (Farbstoffe; Hämoglobin, Cytochrome, Katalase, Rhodopsin), Metallproteine (Metalle; Caeruloplasmin, Transferrin, Ferredoxin u. a. Eisenproteine) u. a. mehr.
| + | Zwei [[Aminosäuren]] können (formal) unter [[Dehydratisierung|Wasserabspaltung]] zu einem Dipeptid kondensieren. |
| | | | |
| − | Vork. u. biolog. Bedeutung: P. sind in der belebten Welt allgegenwärtig. Neben Kohlenhydraten u. Fetten (s. Fette u. Öle) sind sie die dritte große Gruppe von Nahrungs- u. Reservestoffen. Auf der Anwesenheit bestimmter P. beruhen Struktur, Funktion u. Stoffwechsel aller lebenden Zellen u. Gewebe; in gewissem Sinn sind die P. die Träger der Lebensfunktionen schlechthin. Man findet sie gleichermaßen in Tieren, Pflanzen u. Mikroorganismen, so z. B. in den Muskeln (Actin, Myoglobin, Myosin), im Blut (Hämoglobin), in Bindegewebe, Sehnen u. Bändern (Collagen, Elastin), im Serum (Fibrinogen, Immunglobuline, s. a. Plasma- u. Serumproteine), in Wolle, Haaren, Hörnern, Hufen, Klauen, Nägeln usw. (Keratine), in den Seidenfäden (Fibroin), in Weichtierschalen (Conchagene), in Knochen (Ossein), in der Milch (Albumine, Casein) usw. – eine vollständige Aufzählung erscheint weder möglich noch sinnvoll. Der P.-Gehalt tier. u. pflanzlicher Organe ist sehr verschieden, z. B.: Fleisch (Muskelgewebe, Rind) 19%, Fisch 16–18%, Knochen (Rind) 30%, Haut 90–97%, Horn, Klauen, Haare 90–100%, Blut (Mensch) 21%, Milch (Mensch) 1%, (Kuh) 3,2%, (Schaf) 5,6%, Eiklar (Huhn) 12–13%. Pflanzliches P. ist vorwiegend in Samen, Knollen usw. gespeichert, z. B. in Getreidekörnern (10–12%), Lupinensamen (37%), Sojabohnen (36%), Kartoffelknollen (nur 2%).
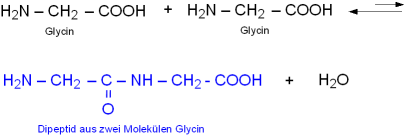
| + | Im Beispiel reagieren zwei Moleküle der einfachsten Aminosäure [[Glycin]] zu einem Dipeptid:[[Bild:Amidbinung.png]] |
| | | | |
| − | Vielfältig sind auch die Funktionen der P. im Organismus: Als Enzyme (Beisp. s. dort), Transport- u. Speichermol. (Ferritin, Hämoglobin), mol. Motoren (Dynein, Kinesin, Myosin), Gerüstsubstanzen (Skleroproteine, Gerüst-Eiweiß) mit mechan. stützenden Funktionen (Keratine, Collagene, Ossein), in der Immunabwehr (Immunglobuline, Komplement), Hormone (Follitropin, Thyreotropin), Hormon- u. Neurotransmitter-Rezeptoren, Regulatoren (Enzym-Inhibitoren, Transkriptionsfaktoren), Schlangengifte, Bakterientoxine, als Reservestoffe (Gliadin, Zein, Edestin) in Pflanzenorganen usw.
| + | ==Struktur der Peptidgruppe== |
| | | | |
| − | Eigenschaften: Die meist gut wasserlösl. P. (Ausnahmen: Membran-P., s. Membranen, u. Skleroproteine) sind gegen physikal. u. chem. Einwirkung im allg. ziemlich empfindlich. So gerinnt z. B. das Hühner-Eiweiß (Eiklar) oberhalb 65 °C; man bezeichnet diesen Vorgang als Denaturierung. Er beruht auf einer Zerstörung der Raumstruktur der P. unter Aufbrechen eines Teils der schwachen innermol. Wechselwirkungen (vgl. den Abschnitt zur Struktur). Im Gegensatz dazu sind die nativen P. (die man z. B. durch Wasser od. Puffersalz-Lsg. aus den Geweben herauslöst) vermutlich noch in dem gleichen Zustand vorhanden wie im Gewebe selber. Denaturierende Agenzien sind z. B. Guanidiniumchlorid, Harnstoff, Natriumdodecylsulfat, elektr. Ladungen, Säuren (Milchgerinnung infolge Milchsäure-Bildung), Schwermetallsalze usw. Schonendere Ausflockungen ohne bedeutende Denaturierung können z. T. durch Alkohol, Ammoniumsalze u. dgl. erreicht werden. Bei dieser Ausfällung erfolgt eine Schwächung der Hydrathülle der Proteine. Bei der Quellung werden Wasser-Mol. von den P.-Mol. gebunden. Bei vielen globulären P. ist auch eine Kältedenaturierung bekannt, d. h. eine Inaktivierung bei Abkühlung der P.-Lösung.
| + | * Bestimmung der Bildungslänge in Peptidbindung durch Röntgenstrukturanalyse |
| | + | * C/N-Bindung ist kürzer als bei [[Amine]]n (Doppelbindungscharakter) |
| | + | * Peptid-Gruppe ist eben gebaut |
| | + | * durch die Delokalisierung der Peptidgruppe wird ein besonders stabiles Verbindungsverhältnis erreicht |
| | + | * [[Carbonyl-Gruppe|Amid-Gruppe]] ist planar gebaut, d. h. alle am Aufbau der der Verbindung beteiligten Atome liegen auf einer Ebene |
| | + | * der Diederwinkel liegt daher bei 180°[[Bild:Pfeil.gif]]Atome können nicht verdreht werden |
| | + | * aus Grenzformeln ergibt sich, dass die C/N-Bindung Doppelbindungscharakter hat und so nicht frei drehbar[[Bild:Pfeil.gif]]Atome der Peptidbindung und benachbarte a-C-Atome sind daher in einer Ebene[[Bild:Pfeil.gif]]starre Struktureinheit |
| | + | * a-C-Atome können zur C/N-Bindung einer Peptid-Gruppe [[cis]] oder [[trans]] angeordnet sein[[Bild:Pfeil.gif]]aus sterischen Gründen meistens [[trans]] |
| | + | * die Ausbildung einer Peptid-Gruppe beeinflusst die Struktur von [[Proteine]]n |
| | + | * Verformungen sind nur an den a-C-Bindungen möglich, da diese[[Bild:Pfeil.gif]]tetraedrisch angeordnet und frei drehbar sind |
| | + | * Möglichkeit der [[Konformation]] ist deshalb bei [[Proteine]]n stark eingeschränkt |
| | | | |
| − | Aufgrund der ionisierbaren Seitenketten der sauren AS Asparaginsäure u. Glutaminsäure (können Anionen bilden), der bas. AS Lysin, Arginin u. Histidin (können Kationen bilden), sowie der freien Amino- u. Carboxy-Gruppe an den Enden der Polypeptid-Kette kommt dem Protein ein amphoterer Charakter zu, u. es nimmt in Abhängigkeit vom pH-Wert eine jeweils verschiedene elektr. Gesamtladung an; der pH-Wert, bei dem diese verschwindet, heißt isoelektr. Punkt. Bei ihm ist die Wasserlöslichkeit des P. am geringsten.
| + | [[Bild:chemie.jpg]] Grenzformeln |
| | + | [[Bild:chemie2.jpg]]delokalisiertes Elektronensystem |
| | | | |
| − | Struktur: Die Elementaranalyse weist bei P. (neben Sauerstoff, in % Trockengew.) Kohlenstoff (50–52%), Wasserstoff (6,8–7,7%), Stickstoff (15–18%) u. Schwefel (0,5–2%) nach. Häufig findet man auch noch Phosphor, gelegentlich auch Spuren von Eisen, Kupfer, Zink, Mangan, Chlor, Brom, Iod u. dgl., die Begleitsubstanzen (Cofaktoren) angehören.
| + | ==Aufgabe== |
| − | AS-Zusammensetzung: Der für P. bes. kennzeichnende Stickstoff-Gehalt ist auf ihre Grundbausteine, die AS, zurückzuführen. Mit Hilfe von Säuren, Laugen od. Enzymen (s. Proteasen) lassen sich alle P. nahezu restlos hydrolyt. in AS zerlegen. Die Analyse dieser Hydrolysate ergibt, daß P. – neben selteneren Aminosäuren (s. dort) – immer wieder dieselben 20 AS enthalten, wenn auch in unterschiedlichen Anteilen u. nicht immer alle zugleich, nämlich Glycin (Gly), L-Alanin (Ala), L-Serin (Ser), L-Cystein (Cys), L-Phenylalanin (Phe), L-Tyrosin (Tyr), L-Tryptophan (Trp), L-Threonin (Thr), L-Methionin (Met), L-Valin (Val), L-Prolin (Pro), L-Leucin (Leu), L-Isoleucin (Ile), L-Lysin (Lys), L-Arginin (Arg), L-Histidin (His), L-Asparaginsäure (Asp), L-Asparagin (Asn), L-Glutaminsäure (Glu) u. L-Glutamin (Gln). Alle opt. aktiven AS der P. haben also L-Konfiguration, was im folgenden bei Nennung einzelner Aminosäuren nicht mehr speziell angegeben wird.
| + | [[Glutathion]] ist ein Tripeptid mit der [[Aminosäuren|Aminosäure]]sequenz (Glu-Cys-Gly). Es schützt in lebenden Zellen Verbindungen vor Oxidation. Dabei wird Glutathion selbst oxidiert. M(Glutathion) = 307 g <b>·</b> mol<sup>-1</sup>; M(Oxidationsprodukt) = 612 g <b>·</b> mol<sup>-1</sup>) |
| | | | |
| − | Peptid-Bindung: Der Zusammenschluß dieser AS zu den hochmol. P. geschieht durch die Bildung von Säureamid-Bindungen zwischen den Carboxy- u. Amino-Gruppen verschiedener AS-Moleküle. Die Zusammensetzung aus AS u. die Art der Bindung, die man als Peptid-Bindung bezeichnet, haben die P. mit den weniger hochmol. Peptiden gemeinsam. Insbes. unterscheidet man diese nach Anzahl der verknüpften AS-Einheiten als Di-, Tri-, Oligo- (bei bis zu 10 AS-Resten) u. Polypeptide (ca. 10–100 AS-Reste). Demnach kann man Peptide u. P. mit der in Abb. 1 dargestellten Strukturformel charakterisieren, die auch zum Ring geschlossen sein kann, s. Cyclopeptide.
| + | a) Gebe die Strukturformel des Tripeptids als [[Zwitterion]] an. Beachte dabei, dass Glutaminsäure im Glutathion eine γ-Peptidbindung ausbildet. |
| | | | |
| − |
| + | b) Leite die Strukturformel des Oxidationsproduktes aus den Angaben der molaren Massen ab. |
| | | | |
| | + | c) Gebe die [[Reaktionsgleichung]] der [[Oxidation]] mit Hilfe der Strukturformeln an und benenne den entstehenden Bindungstyp. |
| | | | |
| − | Peptide
| + | [[Bild:Pfeil.gif]][[Peptidbindung: Antwort]] |
| | | | |
| − | (von griech.: peptos = verdaulich). Bez. für durch Peptid-Bindungen Säureamid-artig verknüpfte Kondensationsprodukte von Aminosäuren.
| + | ==Powerpointpräsentation== |
| | | | |
| − |
| + | http://www.bs-wiki.de/mediawiki/images/Peptidbindung1.ppt |
| | | | |
| − | Abb.: Allg. Strukturformel der Peptide.
| + | ==Versuch== |
| − | Bauen sich die Mol. aus 2 Aminosäure-Resten auf, so spricht man von Dipeptiden, bei 3 u. mehr von Tri-, Tetra-, Pentapeptiden etc.; P. mit 2–10 Aminosäure-Resten faßt man als Oligopeptide, solche mit 10–100 als Polypeptide zusammen, doch ist der Übergang von den letzteren zu den höhermol. Proteinen (Eiweißstoffen) nicht genau definiert. P. mit Bindungen zwischen den seitenständigen Amino-Gruppen von Diaminocarbonsäuren (z. B. Lys) u. seitenständigen Carboxy-Gruppen von Aminodicarbonsäuren (z. B. Glu, Asp) statt der üblichen Peptid-Bindungen zwischen a-NH2 u. -COOH nennt man Isopeptide; die von mehrfunktionellen Aminosäuren wie Glu, Asp, Lys, Arg u. Desmosin ausgehenden zusätzlichen Bindungen sind für die Entstehung von P.-Netzstrukturen verantwortlich. P., deren Aminosäure-Sequenz relativ zu einem bestimmten anderen P. die gegenläufige Reihenfolge an Aminosäuren aufweisen, werden als Retropeptide bezeichnet. Zur Schreibung von P.-Formeln benutzt man meist 1- od. 3-Buchstaben-Notationen für die Aminosäuren, s. die Liste dort. Z. B. stehen AG od. Ala-Gly für L-Alanylglycin [H2N–CH(CH3)–CO–NH–CH2–COOH] u. GA od. Gly-Ala für isomeres Glycyl-L-alanin [H2N–CH2–CO–NH–CH(CH3)–COOH]; falls nicht anders gekennzeichnet (etwa durch: Gly¬Ala), steht links die (freie od. protonierte) Amino-Gruppe u. rechts die (freie od. deprotonierte) Carboxy-Gruppe.
| |
| | | | |
| − | Biolog. Bedeutung: Auf die Bedeutung der makromol. P. für pflanzliche u. tier. Organismen wird bei Proteine ausführlich eingegangen. Eine gleichermaßen spezif. Rolle spielen Oligo- u. Polypeptide im tier. Organismus z. B. als Hormone (Peptidhormone), Wachstumsfaktoren, Cytokine, Neurotransmitter u. Neuromodulatoren (Neuropeptide). Für die physiolog. Wirkung der P. ist neben der Konfiguration die Konformation u. die mol. Dynamik von Bedeutung, u. natürlich benötigen die P., um als Mediatoren wirksam werden zu können, spezif. Rezeptoren. Bei der Zell-vermittelten Immunantwort werden Antigene (Fremd-Proteine) von Antigen-präsentierenden Zellen zu P. (Antigen-Peptide, T-Zell-Epitope) abgebaut, von Histokompatibilitäts-Antigenen komplexiert u. so an der Zelloberfläche den T-Lymphocyten zum „Abtasten“ dargeboten; von außen verabreichte P. (peptide feeding) werden ebenfalls präsentiert. Auch von körpereigenen Proteinen abgeleitete Selbst-P. werden präsentiert, was in der Frühphase der T-Zell-Entwicklung für die Entstehung von Selbst-Toleranz von Bedeutung ist. P.-Ester können für süßen (Aspartame®) od. bitteren Geschmack verantwortlich sein, u. wieder andere P. treten als Toxine pflanzlichen od. tier. Ursprungs in Erscheinung. Auch unter den Antibiotika finden sich eine Reihe von P. (Peptid-Antibiotika ), die z. T. Aminosäuren der „unnatürlichen“ D-Konfiguration enthalten, ggf. auch Hydroxycarbonsäuren, die über Esterbindungen verknüpft sind (Peptolide). Viele der physiolog. aktiven P. liegen als homodete od. heterodete Cyclopeptide vor.
| + | '''Biuret-Reaktion''' |
| | | | |
| | + | Der klassische Nachweis von Proteinen geschieht mit der Biuret-Reaktion. |
| | | | |
| − | Herst.: Auch bei der Synth. ist der zeitliche Aufwand aufgrund der Entwicklung automat. Verf. u. der Festphasen-Technik (Merrifield-Technik) ungleich geringer geworden. Für die Herst. biolog. aktiver u. pharmakolog. nutzbarer P. werden heute neben der chem. Peptid-Synthese in zunehmendem Maße Meth. der Biotechnologie u. Gentechnologie eingesetzt, was z. B. auf dem Gebiet der Peptidhormone bereits zu Erfolgen geführt hat.
| + | '''Chemikalien:''' |
| | + | Eiklar-Lösung (Eiklar u. physiologische [[Kochsalz]]-Lösung, diverse Lebensmittel (Fleisch, Nudeln, Kartoffeln, [[Milch]] u.a.), [[Kupfersulfat]]-Lösung, [[Natronlauge]] ca. 4% |
| | | | |
| − | Biosynth.: Meist durch enzymat. „Resektion“ aus Proteinen, die nach Maßgabe des genetischen Codes (Näheres s. dort) u. der Sequenzinformation der Messenger-Ribonucleinsäuren in den Ribosomen gebildet werden, vgl. Peptidhormone. In manchen Fällen findet jedoch durch nicht-ribosomale Enzyme eine Biosynth. von P. aus den Aminosäuren statt .
| + | '''Geräte:''' |
| | + | Reagenzglas mit Stopfen, [[Reagenzglasständer]], [[Reibschale]] mit Pistill, Tropfpipette, Messpipette 5ml |
| | | | |
| | + | '''Durchführung:''' |
| | + | In das Reagenzglas gibt man etwa 2 mL Eiklar-Lösung. Andere Lebensmittel werden in der Reibeschale zerkleinert, mit wenig Wasser aufgeschlämmt und vorsichtig erwärmt, dann werden etwa 2 mL der Lösung in das Reagenzglas dekantiert. Man gibt nun 2 ml [[Natronlauge]] hinzu, verschließt das Glas mit dem Stopfen und schüttelt gut durch. Jetzt werden 3 Tropfen der Kupfersulfat-Lösung zugefügt. |
| | | | |
| − | ==Peptidbinung==
| + | '''Ergebnis:''' |
| | + | Bei Anwesenheit von Protein entsteht ein gelber Fleck. |
| | | | |
| − | Eine Peptidbindung (-NH-CO-) ist eine Bindung zwischen der Carboxylgruppe einer und der Aminogruppe einer zweiten Aminosäure.
| + | [[Peptidbindung: Versuchsergebnis|Erklärung]] |
| | | | |
| − | Zwei Aminosäuren können (formal) unter Wasserabspaltung zu einem Dipeptid kondensieren.
| |
| | | | |
| − | Im Beispiel reagieren zwei Moleküle der einfachsten Aminosäure Glycin zu einem Dipeptid:[[Bild:Amidbinung.png]]
| + | {{cb|-|375|351}} |
| | | | |
| | + | {{www}} |
| | | | |
| | + | ==Quellen== |
| | + | * Chemie heute, Kapitel 19.8, Seite 375 |
| | + | * Römpp Lexikon Chemie – Version 2.0, Stuttgart/New York: Georg Thieme Verlag 1999 |
| | + | * Versuch aus: Unterricht Chemie, Band 11: Lebensmittel-Nährstoffe, Heinz Schmidkunz, Karin Schlagheck, Aulis Verlag Deubner & Co KG |
| | | | |
| | + | #[[Benutzer:Johannes|Johannes]] |
| | + | #[[Benutzer:Mille|Mille]] |
| | | | |
| − | #Struktur der Peptidgruppe
| + | [[Kategorie:Ernährungslehre]] |
| − | | + | [[Kategorie:Chemie]][[Kategorie:Chemikalien]][[Kategorie:Experiment]] |
| − | Quelle: Chemie heute Seite 375 Kapitel 19.8,Römpp Lexikon Chemie – Version 2.0, Stuttgart/New York: Georg Thieme Verlag 1999
| |
b) Leite die Strukturformel des Oxidationsproduktes aus den Angaben der molaren Massen ab.
Der klassische Nachweis von Proteinen geschieht mit der Biuret-Reaktion.

 Atome können nicht verdreht werden
Atome können nicht verdreht werden Atome der Peptidbindung und benachbarte a-C-Atome sind daher in einer Ebene
Atome der Peptidbindung und benachbarte a-C-Atome sind daher in einer Ebene starre Struktureinheit
starre Struktureinheit aus sterischen Gründen meistens trans
aus sterischen Gründen meistens trans tetraedrisch angeordnet und frei drehbar sind
tetraedrisch angeordnet und frei drehbar sind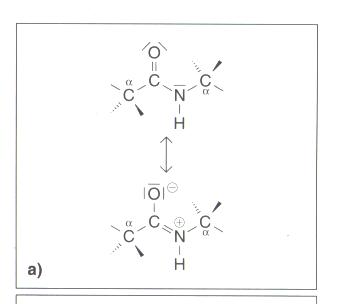 Grenzformeln
Grenzformeln
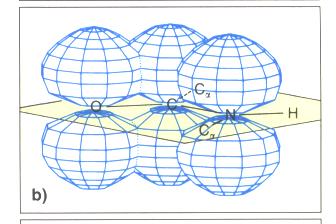 delokalisiertes Elektronensystem
delokalisiertes Elektronensystem



