Halbtitration: Unterschied zwischen den Versionen
Aus BS-Wiki: Wissen teilen
Dg (Diskussion | Beiträge) |
Dg (Diskussion | Beiträge) |
||
| Zeile 1: | Zeile 1: | ||
{{navi|Säure-Base-Titration|Säurestärke}} | {{navi|Säure-Base-Titration|Säurestärke}} | ||
== Zweck == | == Zweck == | ||
| + | [[Bild:Halbtitration.jpg|right]] | ||
Das Ziel einer '''Halbtitration''' ist die [[Experiment|experiment]]elle Bestimmung der [[Säurestärke]] einer schwachen Säure. | Das Ziel einer '''Halbtitration''' ist die [[Experiment|experiment]]elle Bestimmung der [[Säurestärke]] einer schwachen Säure. | ||
| − | + | == Laborpraxis == | |
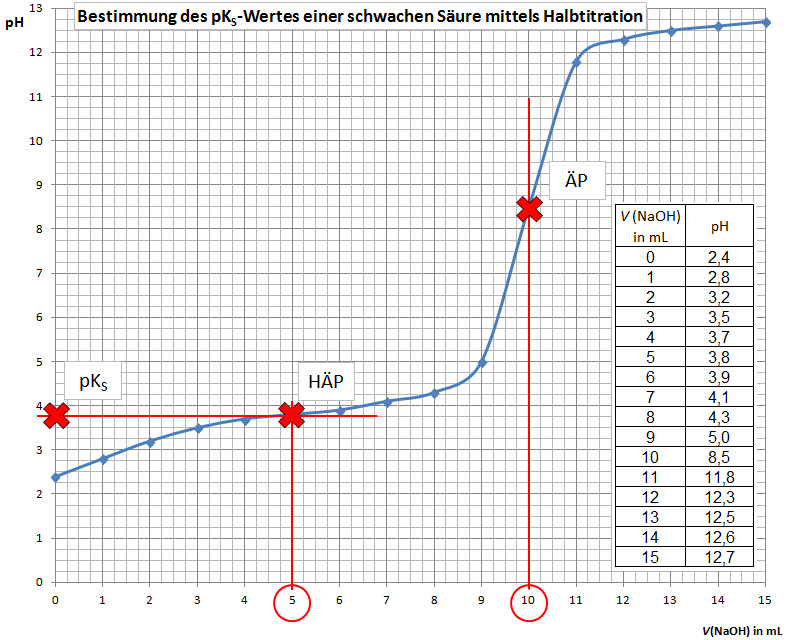
Hierbei wird die schwache Säure mit Natronlauge titriert. Aus der Messreihe (pH-Werte/''V''(NaOH)) wird eine [[Titrationskurve]] erstellt. Aus dieser Titrationskurve kann der pK<sub>S</sub>-Wert der schwachen Säure in abgelesen werden: | Hierbei wird die schwache Säure mit Natronlauge titriert. Aus der Messreihe (pH-Werte/''V''(NaOH)) wird eine [[Titrationskurve]] erstellt. Aus dieser Titrationskurve kann der pK<sub>S</sub>-Wert der schwachen Säure in abgelesen werden: | ||
# Lot fällen vom [[Äquivalenzpunkt]] (ÄP, Wendepunkt der Titrationskurve) | # Lot fällen vom [[Äquivalenzpunkt]] (ÄP, Wendepunkt der Titrationskurve) | ||
Version vom 23. April 2017, 13:18 Uhr
| Halbtitration | ||
|---|---|---|
| vernetzte Artikel | ||
| Säure-Base-Titration | Säurestärke | |
Inhaltsverzeichnis
Zweck
Das Ziel einer Halbtitration ist die experimentelle Bestimmung der Säurestärke einer schwachen Säure.
Laborpraxis
Hierbei wird die schwache Säure mit Natronlauge titriert. Aus der Messreihe (pH-Werte/V(NaOH)) wird eine Titrationskurve erstellt. Aus dieser Titrationskurve kann der pKS-Wert der schwachen Säure in abgelesen werden:
- Lot fällen vom Äquivalenzpunkt (ÄP, Wendepunkt der Titrationskurve)
- V(NaOH) beim ÄP ablesen
- Halbäquivalenzpunkt einzeichnen: Senkrechte einzeichnen bei der Hälfte des NaOH-Verbrauches, der Schnittpunkt mit der Titrationskurve ist der Halbäquivalenzpunkt
- pKS-Wert ablesen: Der pKS-Wert entspricht dem pH-Wert am Halbäquivalenzpunkt.
Experimente
- Bestimmung des pKS-Wertes von Salicylsäure mittels Halbtitration, in: Elemente Chemie 2, Seite 219, Versuch 1
Übungsaufgaben
- Elemente Chemie 2, Seite 219, Aufgabe 1: Bestimmung des pKS-Wertes von Ameisensäure mittels Halbtitration
| Im Chemiebuch ... | ||
|---|---|---|
| findest Du weitere Informationen zum Thema Halbtitration: | ||
Chemie FOS-T
auf Seite |
Chemie heute
auf Seite |
Elemente Chemie
auf Seite |