| Carbonylgruppe | ||
|---|---|---|
| vernetzte Artikel | ||
| Aldehyde | Ketone | |
Definition
Carbonylgruppen sind funktionelle Gruppen in organischen Verbindungen. Sie bestehen aus einem Kohlenstoff- und einem Sauerstoffatom, die durch eine C=O Doppelbindung verknüpft sind.
Die wichtigsten Carbonylgruppen
| Strukturformel | ||
|---|---|---|
| Aldehyde | 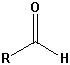 |
|
| Ketone | 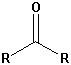 |
|
| Carbonsäuren | 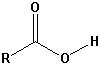 |
|
| Ester | 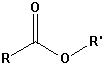 |
|
| Amid (Cyclisches Amid = Lactam) |  |
Man kann diese Carbonylverbindungen in zwei Untergruppen einteilen:
Aldehyde und Ketone können keine negative Ladung tragen, denn sie besitzen weder ein H-Atom noch eine Alkyl- oder Aryl-Gruppe. Aus diesem Grund können sie auch nicht als Abgabgsgruppe dienen.
Aldehyde und Ketone verfügen über ähnliche chemische Eigenschaften wie Carbonsäurederivate, unterscheiden sich aber dennoch von ihnen.
2. Acyl-Rest (RCO) in Carbonsäuren und ihre Derivate
Acyl-Rest (RCO) in Carbonsäuren und ihre Derivate sind elektronegative Heteroatome, sie tragen also eine negative Ladung und können aus diesem Grund als Abgangsgruppe dienen. Die Chemie dieser Carbonylverbindungen ist deshalb untereinander ähnlich, weisen aber dennoch einige Unterschiede in ihren chemischen Eigenschaften auf.
Carbonylverbindungen
Aldehyde und Ketone werden als Carbonylverbindungen bezeichnet, da sie beide die Carbonylgruppe als Strukturelement besitzen. Carbonylverbindungen mit einer endständigen Carbonyl-Gruppe werden als Aldehyde bezeichnet. Verbindungen, bei denen die Carbonyl-Gruppe nicht endständig ist, heißen Ketone.
Sie sind auch in der Natur zu finden, zum Beispiel spielen 28 verschiedene Carbonylverbindungen und deren Derivate eine große Rolle als Duftstoffe von Erdbeeren, Wein und auch Blumen.
Formaldehyd und seine Verwendung
Additionsreaktionen
Als ungesättigte Verbindungen sind Aldehyde und Ketone reaktionfreudig. Es kommt zu sogenannten Additionsreaktionen, wobei die nucleophile Additon mit Hydronium-Ionen charakteristisch ist. Als Reaktionspartner dienen hierbei Alkohole, Wasser und Anionen.
Die Addition von Alkoholen an Carbonyl-Verbindungen läuft in zwei Schritten ab:
1. Schritt:
Das Sauerstoff-Atom der Carbonylgruppe wird protoniert, d.h. ein Proton wird ihm abgenommen, wodurch es eine negative Ladung bekommt. Mit dem freien Elektronenpaar dieses Sauerstoff-Atoms greift das Alkohol-Molekül nun das Carbonyl-C-Atom nucleophil an. Das Alkohol kann also aufgrund seiner negativen Ladung das positiv geladene Carbonyl-C-Atom angreifen und ihm ein Proton entreißen. Aus einem Aldehyd wird so ein Halbacetal, aus einem Keton bildet sich auf diesem Weg ein Halbketal. Diese Moleküle besitzen die Eigenschaft, dass an einem ihrer C-Atome eine OH- sowie eine Ether-Gruppe sitzt.
2. Schritt:
In diesem Schritt ist es möglich, dass die OH-Gruppe des Halbacetals/Halbketals protoniert wird, im Anschluss daran wird ein H2O-Molekül eliminiert. Folge: ein Acetal/Ketal entsteht. Ihre Bildung ist häufig durch ihren angenehmen Geruch erkennbar.
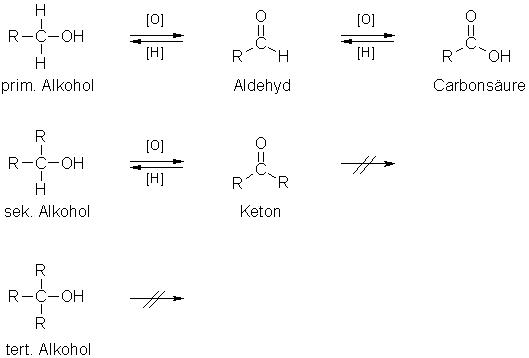
Oxidation & Reduktion der Carbonyl-Gruppe
Die Carbonyl-Gruppe von Aldehyden und Ketonen können oxidiert und reduziert werden, je nach ihrer Oxidationszahl. Aldehyde (Oxidationszahl I) lassen sich sehr gut oxidieren, bei Ketonen (Oxidationszahl II) funktioniert dies nur, wenn zuvor Bindungen gespalten wurden. Ketone wiederum lassen sich gut reduzieren, da sie die Oxidationszahl II haben. Auf diesem Wege kann gut experimentell zwischen Aldehyden und Ketonen unterschieden werden (siehe Versuch).
Oxidation und Reduktion von Carbonyl-Gruppen:
Versuch
Die FEHLING-Probe:
Geeignet für die Durchführung in kleinen Gruppen (3-4 Personen)
Geräte:
- Becherglas (250 ml)
- Kunststoffspritze (5 ml)
- Reagenzgläser
Chemikalien:
- Fehlingsche Lösung I und II
- Propinonaldehyd (1 ml)
- Glucose-Lösung
- Aceton
Sicherheitsmaßnahmen:
- Schutzbrille
- evtl. Schutzhandschuhe
Durchführung:
- Ein Gemisch aus je 5 ml FEHLING-Lösung I und II und 1 ml Propionaldehyd wird in einem Becherglas erhitzt.
- Der Versuchsaufbau wird noch einmal genau so nachgestellt, diesmal jedoch anstatt Propionaldehyd Glucose-Lösung verwenden.
Zu beantworten:
- Welche Beobachtungen machest Du?
- Wie lässt sich die Reaktion erklären?
Aufgaben
- Vergleiche die C=C-Zweifachbindung mit der C=O-Zweifachbindung hinsichtlich Bindungslänge, Bindungsenergie und Polarität.
- Vergleiche Alkane, Alkanole und Alkanale hinsichtlich ihrer Siedetemperatur und ihrer Wasserlöslichkeit. Begründe Deine Aussagen.
Quellen
Bücher:
- Chemie heute - Sekundarbereich II, Schroedel Verlag, Kapitel 14.5, Seite 262-264
Internet:
- http://de.wikipedia.org/wiki/Formaldehyd
- http://www.oci.unizh.ch
- http://www.chemgapedia.de
- http://www-oc.chemie.uni-regensburg.de/OCP/bio/oc2/ws02/Vorlsg-kap04.pdf
- Einige der verwandten internen Links bedienen sich schon vorhandenen Wikiseiten, andere wurden selbst verfasst.
| Im Chemiebuch ... | ||
|---|---|---|
| findest Du weitere Informationen zum Thema Carbonylgruppe: | ||
Chemie FOS-T
auf Seite |
Chemie heute
auf Seite |
Elemente Chemie
auf Seite |