Redoxpotentiale: Übungsaufgaben
Aus BS-Wiki: Wissen teilen
Version vom 23. März 2011, 15:34 Uhr von Dg (Diskussion | Beiträge) (Die Seite wurde neu angelegt: == Abhängigkeit vom pH-Wert == Eine Lösung enthält Dichromat-Ionen mit ''c''(Cr<sub>2</sub>O<sub>7</sub><sup>2-</sup>) = 0,1 mol/L und Chrom(III)-Ionen mit c(Cr<sup...)
Abhängigkeit vom pH-Wert
Eine Lösung enthält Dichromat-Ionen mit c(Cr2O72-) = 0,1 mol/L und Chrom(III)-Ionen mit c(Cr3+) = 0,001 mol/L. Die Lösung wird durch Säurezugabe angesäuert. Berechne das Redoxpotential dieses Redoxpaares bei a) pH = 7; b) pH =1; c) pH = 3.
1. Reaktionsgleichung formulieren:
- Cr2O72- + 14 H+ + 6 e-
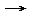 2 Cr3+ + 7 H2O
2 Cr3+ + 7 H2O
2. Standard-Elektrodenpotential aus Spannungsreihe ermitteln: UH°(Cr³+/Cr2O7²+) = 1,33V