Aggregatzustand: Unterschied zwischen den Versionen
Dg (Diskussion | Beiträge) |
Dg (Diskussion | Beiträge) |
||
| Zeile 1: | Zeile 1: | ||
| − | + | Zustandsformen der Materie | |
Bereits im Altertum unterschied man zwischen dem festen, flüssigen u. gasf. Zustand der Materie u. brachte diese mit den drei „Elementen“ Erde, Wasser u. Luft in Beziehung. Im festen A. besitzt die Materie den höchsten Ordnungsgrad. Es überwiegen die anziehenden Kräfte zwischen den Atomen, wodurch diese an feste Plätze in dem Gefüge gebunden sind. Die meisten Festkörper haben krist. Struktur, d. h. eine bestimmte Grundstruktur (Basisgitter) wiederholt sich in regelmäßigem Abstand. | Bereits im Altertum unterschied man zwischen dem festen, flüssigen u. gasf. Zustand der Materie u. brachte diese mit den drei „Elementen“ Erde, Wasser u. Luft in Beziehung. Im festen A. besitzt die Materie den höchsten Ordnungsgrad. Es überwiegen die anziehenden Kräfte zwischen den Atomen, wodurch diese an feste Plätze in dem Gefüge gebunden sind. Die meisten Festkörper haben krist. Struktur, d. h. eine bestimmte Grundstruktur (Basisgitter) wiederholt sich in regelmäßigem Abstand. | ||
Im gasförmigen A. liegt keine räumliche Ordnung mehr vor. Anziehende Kräfte zwischen den Teilchen sind, bei Abständen größer als einige nm, nicht mehr vorhanden. Die Eigenschaften der Substanz sind allein durch die Wärmebewegung gegeben (Brownsche Molekularbewegung). Gase füllen den ihnen zur Verfügung stehenden Raum gleichmäßig aus. | Im gasförmigen A. liegt keine räumliche Ordnung mehr vor. Anziehende Kräfte zwischen den Teilchen sind, bei Abständen größer als einige nm, nicht mehr vorhanden. Die Eigenschaften der Substanz sind allein durch die Wärmebewegung gegeben (Brownsche Molekularbewegung). Gase füllen den ihnen zur Verfügung stehenden Raum gleichmäßig aus. | ||
| + | |||
| + | [[Bild:Aggregat.jpg]] | ||
Als weiterer A. wird der [[Plasma-Zustand]] angesehen. | Als weiterer A. wird der [[Plasma-Zustand]] angesehen. | ||
| − | Welchen A. ein Stoff einnimmt ist von seiner Art, der Temp. u. dem [[Druck]] abhängig. | + | Welchen A. ein Stoff einnimmt, ist von seiner Art, der Temp. u. dem [[Druck]] abhängig. |
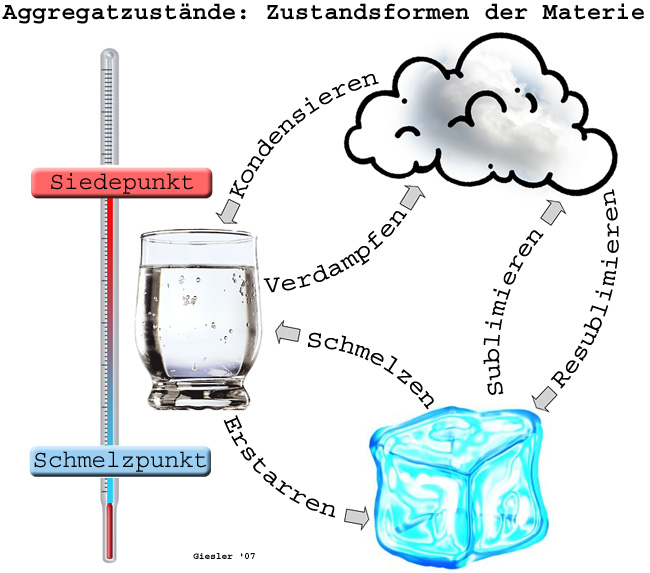
Man kann durch Temp.-Erhöhung vom festen in den flüssigen A. ('''Schmelzen''', hierzu ist die Schmelzwärme aufzuwenden) u. weiter vom flüssigen in den gasf. A. gelangen ('''Verdampfen''', Verdampfungswärme notwendig). Die Temp.-Werte, bei denen diese Übergänge bei [[Normalbedingungen]] (p = 101,3 kPascal) stattfinden, werden als Schmelztemp. (Schmelzpunkt, Schmp.) bzw. Siedetemp. (Siedepunkt, Sdp.) bezeichnet. Beim entgegengesetzten Abkühlprozeß spricht man vom '''Erstarren''' (Erstarrungspunkt) bzw. '''Kondensieren''' (Kondensationspunkt). | Man kann durch Temp.-Erhöhung vom festen in den flüssigen A. ('''Schmelzen''', hierzu ist die Schmelzwärme aufzuwenden) u. weiter vom flüssigen in den gasf. A. gelangen ('''Verdampfen''', Verdampfungswärme notwendig). Die Temp.-Werte, bei denen diese Übergänge bei [[Normalbedingungen]] (p = 101,3 kPascal) stattfinden, werden als Schmelztemp. (Schmelzpunkt, Schmp.) bzw. Siedetemp. (Siedepunkt, Sdp.) bezeichnet. Beim entgegengesetzten Abkühlprozeß spricht man vom '''Erstarren''' (Erstarrungspunkt) bzw. '''Kondensieren''' (Kondensationspunkt). | ||
Version vom 22. Februar 2007, 22:42 Uhr
Zustandsformen der Materie
Bereits im Altertum unterschied man zwischen dem festen, flüssigen u. gasf. Zustand der Materie u. brachte diese mit den drei „Elementen“ Erde, Wasser u. Luft in Beziehung. Im festen A. besitzt die Materie den höchsten Ordnungsgrad. Es überwiegen die anziehenden Kräfte zwischen den Atomen, wodurch diese an feste Plätze in dem Gefüge gebunden sind. Die meisten Festkörper haben krist. Struktur, d. h. eine bestimmte Grundstruktur (Basisgitter) wiederholt sich in regelmäßigem Abstand.
Im gasförmigen A. liegt keine räumliche Ordnung mehr vor. Anziehende Kräfte zwischen den Teilchen sind, bei Abständen größer als einige nm, nicht mehr vorhanden. Die Eigenschaften der Substanz sind allein durch die Wärmebewegung gegeben (Brownsche Molekularbewegung). Gase füllen den ihnen zur Verfügung stehenden Raum gleichmäßig aus.
Als weiterer A. wird der Plasma-Zustand angesehen. Welchen A. ein Stoff einnimmt, ist von seiner Art, der Temp. u. dem Druck abhängig.
Man kann durch Temp.-Erhöhung vom festen in den flüssigen A. (Schmelzen, hierzu ist die Schmelzwärme aufzuwenden) u. weiter vom flüssigen in den gasf. A. gelangen (Verdampfen, Verdampfungswärme notwendig). Die Temp.-Werte, bei denen diese Übergänge bei Normalbedingungen (p = 101,3 kPascal) stattfinden, werden als Schmelztemp. (Schmelzpunkt, Schmp.) bzw. Siedetemp. (Siedepunkt, Sdp.) bezeichnet. Beim entgegengesetzten Abkühlprozeß spricht man vom Erstarren (Erstarrungspunkt) bzw. Kondensieren (Kondensationspunkt).