Anode: Unterschied zwischen den Versionen
Aus BS-Wiki: Wissen teilen
Dg (Diskussion | Beiträge) |
Dg (Diskussion | Beiträge) |
||
| Zeile 3: | Zeile 3: | ||
eine Elektronenabgabe (also eine [[Oxidation]]) erfolgt. Die Polung ist | eine Elektronenabgabe (also eine [[Oxidation]]) erfolgt. Die Polung ist | ||
dabei von der Betriebsart abhängig: | dabei von der Betriebsart abhängig: | ||
| − | * Bei der [[Elektrolyse]] entspricht die Anode dem [[Pluspol]]. Dieser zieht die [[Anionen|negativ geladenen Ionen]] aus der Lösung an und entreißt ihnen Elektronen, die Ionen werden oxidiert, die Elektrode (vereinfachend) bleibt chemisch unverändert, weil die Elektronen im äußeren Stromkreis abgeleitet werden.[[Bild:Elektroden.jpg|right]] | + | * Bei der [[Elektrolyse]] entspricht die Anode dem [[Pluspol]]. Dieser zieht die [[Anionen|negativ geladenen Ionen]] aus der Lösung an und entreißt ihnen Elektronen, die Ionen werden oxidiert, die Elektrode (vereinfachend) bleibt chemisch unverändert, weil die Elektronen im äußeren Stromkreis abgeleitet werden. Kurz: Die Anode ist der Ort der Oxidation von Substanzen.[[Bild:Elektroden.jpg|right]] |
* In [[galvanisches Element|galvanischen Elementen]] wie z. B. der [[Brennstoffzelle]] entspricht die Anode dem [[Minuspol]]. Im Gegensatz zur Elektrolyse ist also das Anodenmaterial selbst Reaktionspartner, d. h. ein z. B. unedles Anoden-Metall bildet durch Elektronenabgabe [[Kationen|positiv geladenen Ionen]] und wird dabei oxidiert. | * In [[galvanisches Element|galvanischen Elementen]] wie z. B. der [[Brennstoffzelle]] entspricht die Anode dem [[Minuspol]]. Im Gegensatz zur Elektrolyse ist also das Anodenmaterial selbst Reaktionspartner, d. h. ein z. B. unedles Anoden-Metall bildet durch Elektronenabgabe [[Kationen|positiv geladenen Ionen]] und wird dabei oxidiert. | ||
Version vom 21. Januar 2018, 16:52 Uhr
In der Chemie ist diejenige Elektrode als Anode definiert, an der eine Elektronenabgabe (also eine Oxidation) erfolgt. Die Polung ist dabei von der Betriebsart abhängig:
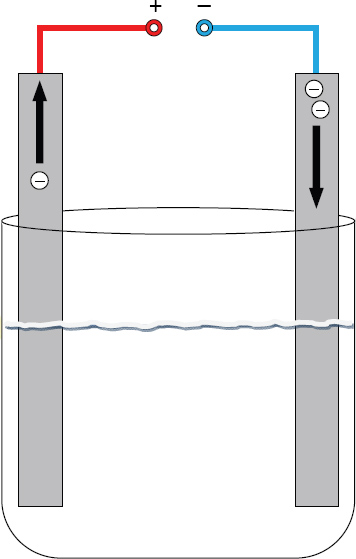
- Bei der Elektrolyse entspricht die Anode dem Pluspol. Dieser zieht die negativ geladenen Ionen aus der Lösung an und entreißt ihnen Elektronen, die Ionen werden oxidiert, die Elektrode (vereinfachend) bleibt chemisch unverändert, weil die Elektronen im äußeren Stromkreis abgeleitet werden. Kurz: Die Anode ist der Ort der Oxidation von Substanzen.
- In galvanischen Elementen wie z. B. der Brennstoffzelle entspricht die Anode dem Minuspol. Im Gegensatz zur Elektrolyse ist also das Anodenmaterial selbst Reaktionspartner, d. h. ein z. B. unedles Anoden-Metall bildet durch Elektronenabgabe positiv geladenen Ionen und wird dabei oxidiert.
Der Name Anode leitet sich vom griech. anodos ab und bedeutet aufwärts führender Weg und geht von der Vorstellung aus, dass die Elektronen durch den Elektronensog an der Anode aus der Lösung in die Anode geleitet werden (Elektrolyse) bzw. aus der Anode in den äußeren Stromkreis (galvanisches Element), siehe Bild.