Redoxpotentiale: Übungsaufgaben: Unterschied zwischen den Versionen
Aus BS-Wiki: Wissen teilen
Dg (Diskussion | Beiträge) |
Dg (Diskussion | Beiträge) |
||
| Zeile 12: | Zeile 12: | ||
3. Einsetzen der Zahlenwerte in die Nernstsche Gleichung: | 3. Einsetzen der Zahlenwerte in die Nernstsche Gleichung: | ||
| − | : ''U<sub>H</sub>(Ox/Red)'' = ''U<sub>H</sub><sup>0</sup>(Ox/Red)'' + 0,059 V/''z''{{*}}log<sub>10</sub> ''c''(Ox)/''c''(Red) | + | : ''U<sub>H</sub>(Ox/Red)'' = ''U<sub>H</sub><sup>0</sup>(Ox/Red)'' + (0,059 V/''z''){{*}}log<sub>10</sub> ''c''(Ox)/''c''(Red) |
4. Unter Berücksichtigung des pH-Wertes ergibt sich nach den Regeln des [[Massenwirkungsgesetz]]es in saurer Lösung: | 4. Unter Berücksichtigung des pH-Wertes ergibt sich nach den Regeln des [[Massenwirkungsgesetz]]es in saurer Lösung: | ||
| − | : ''U<sub>H</sub>(Ox/Red)'' = 1,33 V + 0,059 V/6{{*}}log<sub>10</sub> [''c''(Cr<sub>2</sub>O<sub>7</sub><sup>2-</sup>){{*}}''c''(H<sup>+</sup>)<sup>14</sup>/''c''(Cr<sup>3+</sup>)<sup>2</sup>] | + | : ''U<sub>H</sub>(Ox/Red)'' = 1,33 V + (0,059 V/6){{*}}log<sub>10</sub> [''c''(Cr<sub>2</sub>O<sub>7</sub><sup>2-</sup>){{*}}''c''(H<sup>+</sup>)<sup>14</sup>/''c''(Cr<sup>3+</sup>)<sup>2</sup>] |
a) für pH = 7 gilt damit: | a) für pH = 7 gilt damit: | ||
| − | : ''U<sub>H</sub>(Ox/Red)'' = 1,33 V + 0,059 V/6{{*}}log<sub>10</sub> [0,1{{*}}(10<sup>-7</sup>)<sup>14</sup> / (10<sup>-3</sup>)<sup>2</sup>] = 1,33 V + 0,059 V/6{{*}}log<sub>10</sub> | + | : ''U<sub>H</sub>(Ox/Red)'' = 1,33 V + (0,059 V/6){{*}}log<sub>10</sub> [0,1{{*}}(10<sup>-7</sup>)<sup>14</sup> / (10<sup>-3</sup>)<sup>2</sup>] |
| + | Zehnerpotenzen zusammenfassen: | ||
| + | : ''U<sub>H</sub>(Ox/Red)'' = 1,33 V + (0,059 V/6){{*}}log<sub>10</sub>[10<sup>12</sup>] | ||
| + | Zwischenergebnis: | ||
| + | : ''U<sub>H</sub>(Ox/Red)'' = 1,33 V + (0,059 V/6){{*}}12 | ||
| + | Ausrechnen: | ||
| + | : ''U<sub>H</sub>(Ox/Red)'' = 1,33 V + (0,059 V/6){{*}}12 | ||
[[Kategorie:Chemie]] | [[Kategorie:Chemie]] | ||
Version vom 23. März 2011, 17:30 Uhr
Abhängigkeit vom pH-Wert
Eine Lösung enthält Dichromat-Ionen mit c(Cr2O72-) = 0,1 mol/L und Chrom(III)-Ionen mit c(Cr3+) = 0,001 mol/L. Die Lösung wird durch Säurezugabe angesäuert. Berechne das Redoxpotential dieses Redoxpaares bei a) pH = 7; b) pH =1; c) pH = 3.
1. Reaktionsgleichung formulieren und Anzahl z der übertragenen Elektronen ermitteln:
- Cr2O72- + 14 H+ + 6 e-
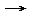 2 Cr3+ + 7 H2O
2 Cr3+ + 7 H2O - z = 6
2. Standard-Elektrodenpotential UH0 des Redoxpaares (Ox/Red) aus Spannungsreihe ermitteln (z. B. Chemie heute, S. 141):
- UH0(Cr2O72-/Cr3+) = 1,33 V
3. Einsetzen der Zahlenwerte in die Nernstsche Gleichung:
- UH(Ox/Red) = UH0(Ox/Red) + (0,059 V/z) · log10 c(Ox)/c(Red)
4. Unter Berücksichtigung des pH-Wertes ergibt sich nach den Regeln des Massenwirkungsgesetzes in saurer Lösung:
- UH(Ox/Red) = 1,33 V + (0,059 V/6) · log10 [c(Cr2O72-) · c(H+)14/c(Cr3+)2]
a) für pH = 7 gilt damit:
- UH(Ox/Red) = 1,33 V + (0,059 V/6) · log10 [0,1 · (10-7)14 / (10-3)2]
Zehnerpotenzen zusammenfassen:
- UH(Ox/Red) = 1,33 V + (0,059 V/6) · log10[1012]
Zwischenergebnis:
- UH(Ox/Red) = 1,33 V + (0,059 V/6) · 12
Ausrechnen:
- UH(Ox/Red) = 1,33 V + (0,059 V/6) · 12