Oxidation: Unterschied zwischen den Versionen
Aus BS-Wiki: Wissen teilen
Dg (Diskussion | Beiträge) |
Dg (Diskussion | Beiträge) |
||
| Zeile 1: | Zeile 1: | ||
| − | {{navi|Redoxreaktion| | + | {{navi|Redoxreaktion|Reaktionstyp}} |
Eine Oxidation ist: | Eine Oxidation ist: | ||
Version vom 20. März 2010, 20:56 Uhr
| Oxidation | ||
|---|---|---|
| vernetzte Artikel | ||
| Redoxreaktion | Reaktionstyp | |
Eine Oxidation ist:
- das Gegenteil zur Reduktion, findet aber zeitgleich statt (siehe Redoxreaktion)
- einer vereinfachenden Definition nach eine Reaktion mit Sauerstoff, siehe Verbrennung
- im erweiterten Sinne eine Reaktion, bei der Elektronen abgegeben werden (Elektronen-Abgabe), z. B. an den Sauerstoff oder an einen anderen Reaktionspartner mit einer höheren Elektronegativität, zum Beispiel Chlor.
Mg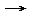 Mg2+ + 2e-, hierbei geht die O. mit einer Erhöhung der Oxidationszahl einher, im Beispiel von 0 auf 2.
Mg2+ + 2e-, hierbei geht die O. mit einer Erhöhung der Oxidationszahl einher, im Beispiel von 0 auf 2.
Der Stoff, der Elektronen aufnimmt (zum Beispiel: Chlor), wird als Oxidationsmittel bzw. Elektronen-Akzeptor ("Nehmer") bezeichnet.
