Carbonylgruppe: Unterschied zwischen den Versionen
(→Carbonylverbindungen) |
(→Die Wichtigsten Carbonylgruppen) |
||
| Zeile 33: | Zeile 33: | ||
| [[Bild:Amid1.JPG]]|| | | [[Bild:Amid1.JPG]]|| | ||
|} | |} | ||
| + | |||
| + | Man kann diese Carbonylverbindungen in zwei Untergruppen einteilen: | ||
| + | |||
| + | #Aldehyde und Ketone | ||
| + | |||
| + | Aldehyde und Ketone können keine negative Ladung tragen, da sie entweder ein H-Atom oder eine Alkyl- oder Aryl-Gruppe besitzen. | ||
| + | Daher können sie nicht als Abgangsgruppe dienen. | ||
| + | Sie besitzen ähnliche chemische Eigenschaften, unterscheiden sich aber von den Carbonsäurederivaten. | ||
| + | |||
| + | #Acyl-Rest (RCO) in Carbonsäuren und ihren Derivaten | ||
| + | |||
| + | Diese elektronegativen Heteroatome können eine negative | ||
| + | Ladung tragen und können deswegen als Abgangsgruppen dienen. | ||
| + | Die Chemie dieser Carbonylverbindungen ist deswegen | ||
| + | untereinander ähnlich. | ||
== Carbonylverbindungen == | == Carbonylverbindungen == | ||
Version vom 28. November 2006, 17:22 Uhr
Inhaltsverzeichnis
Definition
Carbonylgruppen sind chemische Gruppen in organischen Verbindungen. Sie bestehen aus einem Kohlenstoff- und einem Sauerstoffatom, die durch eine C=O Doppelbindung verknüpft sind. Die Carbonylgruppe ist die funktionelle Gruppe und gleichzeitig das charakteristische Merkmal für die Aldehyde und Ketone.
Die Wichtigsten Carbonylgruppen
| Strukturformel | ||
|---|---|---|
| Aldehyd | 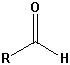 |
|
| Keton | 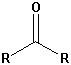 |
|
| Carbonsäure | 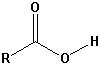 |
|
| Alkanoylhalogenid | Datei:Alkano1.JPG | |
| Anhydrid | Datei:Anhyd1.JPG | |
| Ester | 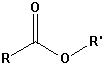 |
|
| Lacton (Cyclische Ester) | Datei:Lacton1.JPG | |
| Amid (Cyclisches Amid = Lactam) |  |
Man kann diese Carbonylverbindungen in zwei Untergruppen einteilen:
- Aldehyde und Ketone
Aldehyde und Ketone können keine negative Ladung tragen, da sie entweder ein H-Atom oder eine Alkyl- oder Aryl-Gruppe besitzen. Daher können sie nicht als Abgangsgruppe dienen. Sie besitzen ähnliche chemische Eigenschaften, unterscheiden sich aber von den Carbonsäurederivaten.
- Acyl-Rest (RCO) in Carbonsäuren und ihren Derivaten
Diese elektronegativen Heteroatome können eine negative Ladung tragen und können deswegen als Abgangsgruppen dienen. Die Chemie dieser Carbonylverbindungen ist deswegen untereinander ähnlich.
Carbonylverbindungen
Aldehyde und Ketone werden als Carbonylverbindungen bezeichnet, da sie beide die Carbonylgruppe als Strukturelement besitzen.
Sie sind auch in der Natur zu finden, zum Beispiel spielen 28 verschiedene Carbonylverbindungen und deren Derivate eine große Rolle als Duftstoffe von Erdbeeren, Wein und auch Blumen.
Verwendung von Formaldehyd
Für Formaldehyd, welches eine Carbonyl-Gruppe enthält, ist unter anderem einer der wichtigsten Grundstoffe der chemischen Industrie und dient auch als Ausgangsstoff für viele andere chemische Verbindungen, der größte Teil des hergestellten Formaldehyds wird jedoch zur Herstellung von Kunststoffen wie Aminoplasten und Phenoplasten genutzt.
Außerdem wird es bei der Textilveredelung und bei der Herstellung Farbstoffen und Pharmaka verwandt, sowie als Konservierungsstoff für verderbliche Güter wie Kosmetika.
Diese Verwendung gilt jedoch als problematisch und auch als umstritten, da Formaldehyd hautreizend ist. Es gilt auch als krebserrebgend, da die Formaldehyd-Moleküle bei höheren Konzentrationen in die Zelle oder den Zellkern eindringen können und dort mit den NH2-Gruppen der Nucleinsäure reagieren. Dardurch können Schäden hervorgerufen werden, die zu krebsartigen Entartung führen können.
Additionsreaktionen
Da Aldehyde und Ketone ungesättigte Verbindungen sind, sie also die Edelgaskonfiguration anstreben, sind sie sehr reaktionfreudig. Es kommt zu sogenannten Additionsreaktionen, wobei die nucleophile Additon mit Hydronium-Ionen charakteristisch ist. Als Reaktionspartner dienen hierbei Alkohole, Wasser und Anionen.
Die Addition von Alkoholen an Carbonyl-Verbindungen läuft in zwei Schritten ab:
- Schritt: Nachdem das Sauerstoff-Atom der Carbvonylgruppe protoniert, also
Oxidation & Reduktion der Carbonyl-Gruppe
Versuch
Aufgaben
Quellen
Bücher:
- Chemie heute - Sekundarbereich II, Schroedel Verlag, Kapitel 14.5, Seite 262-264
Internet:
14.5/6
