Thiazolgelb: Unterschied zwischen den Versionen
Dg (Diskussion | Beiträge) |
Dg (Diskussion | Beiträge) |
||
| (8 dazwischenliegende Versionen desselben Benutzers werden nicht angezeigt) | |||
| Zeile 1: | Zeile 1: | ||
| − | '''Thiazolgelb''', auch Titangelb ({{ci|19540}}), ist ein gelb-brauner Farbstoff, der als [[Fluoreszenz]]-[[Indikator]] und als [[ | + | '''Thiazolgelb''', auch Titangelb ({{ci|19540}}), ist ein gelb-brauner Farbstoff, der als [[Fluoreszenz]]-[[Indikator]] und als [[Metallindikator]] auf [[Magnesium]] verwendet wird. |
[[Titan]] ist ''nicht'' in dieser Substanz enthalten. | [[Titan]] ist ''nicht'' in dieser Substanz enthalten. | ||
== Eigenschaften == | == Eigenschaften == | ||
| − | Bei einem [[pH-Wert]] zwischen 12,0 und 13,0 schlägt das Gelb in ein Rot (bzw. Braungelb) um.{{Indikator|Menge=0,1|LM= | + | Bei einem [[pH-Wert]] zwischen 12,0 und 13,0 schlägt das Gelb in ein Rot (bzw. Braungelb) um.{{Indikator|Menge=0,1|LM=dest. Wasser|R=gilt als unbedenklich.}} |
{{UVV-C|9991949}} | {{UVV-C|9991949}} | ||
== Magnesium-Nachweis == | == Magnesium-Nachweis == | ||
| − | + | Viele andere Metall-Ionen (vor allem [[Aluminium]], [[Arsen]], [[Bismut]], [[Cobalt]], [[Mangan]], [[Nickel]], [[Zinn]], [[Zink]]) stören diesen Nachweis und müssen vorab als [[Sulfid]]e [[Fällung|gefällt]] werden. | |
| − | + | ||
| + | 5 mL der Mg-haltigen Lösung mit 5 Tropfen der Titangelb-Lösung versetzen und mit 5 mL [[Natronlauge]] (''[[Stoffmengenkonzentration|c]]'' = 1 mol/L) alkalisch machen. Bei Anwesenheit von Magnesium-Ionen entsteht nach ca. 2 Minuten ein hellroter Niederschlag. | ||
| + | {{UW|112|Qualitativer Nachweis von Magnesium}} | ||
| + | {{NiU|120|11 (2010)|Sabine Venke und Wolfgang Proske: Nachweis von Magnesiumionen in Spinat}} | ||
[[Kategorie:Chemie]][[Kategorie:Chemikalien]] | [[Kategorie:Chemie]][[Kategorie:Chemikalien]] | ||
[[Kategorie:Reagenzien]] | [[Kategorie:Reagenzien]] | ||
Aktuelle Version vom 22. März 2017, 12:32 Uhr
Thiazolgelb, auch Titangelb (C.I. 19540), ist ein gelb-brauner Farbstoff, der als Fluoreszenz-Indikator und als Metallindikator auf Magnesium verwendet wird.
Titan ist nicht in dieser Substanz enthalten.
Inhaltsverzeichnis
Eigenschaften
Bei einem pH-Wert zwischen 12,0 und 13,0 schlägt das Gelb in ein Rot (bzw. Braungelb) um.| Thiazolgelb | ||
|---|---|---|
| vernetzte Artikel | ||
| Indikatoren | pH-Skala | |
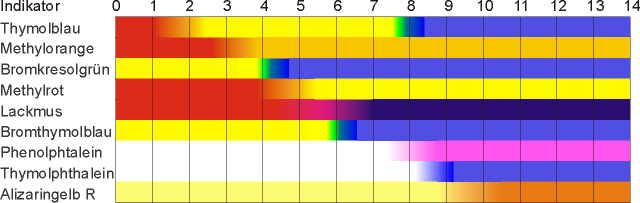
Thiazolgelb ist ein Säure/Base-Indikator mit charakteristischem Farbwechsel bei bestimmten pH-Werten.
Diese Umschlagbereiche und den Vergleich mit anderen Indikatoren zeigt das folgende Bild:
Thiazolgelb-Lösung
Übliche Konzentration: 0,1 g Thiazolgelb in 100 mL dest. Wasser lösen.
Sicherheitshinweise
Bei der Verwendung von Thiazolgelb beim Experimentieren gilt:
| |
Auf Chemikalien-Gefäßen finden sich codierte Hinweise auf Gefährdungen und entsprechende Vorsorgemaßnahmen beim Umgang mit dieser Chemikalie. Diese sogenannten H- & P-Sätze hängen gemeinsam mit den Arbeitsregeln für Schülerexperimente als Betriebsanweisung im Chemieraum aus und müssen in jedem Fall beachtet werden! |
Thiazolgelb gilt als unbedenklich.
Weblinks
- Thiazolgelb als Google-Suchbegriff
- Thiazolgelb in der Wikipedia
- Thiazolgelb hier in bs-wiki.de mit Google
- Thiazolgelb als Youtube-Video
- Sicherheitsdatenblatt von Thiazolgelb unseres Lieferanten Conatex
Magnesium-Nachweis
Viele andere Metall-Ionen (vor allem Aluminium, Arsen, Bismut, Cobalt, Mangan, Nickel, Zinn, Zink) stören diesen Nachweis und müssen vorab als Sulfide gefällt werden.
5 mL der Mg-haltigen Lösung mit 5 Tropfen der Titangelb-Lösung versetzen und mit 5 mL Natronlauge (c = 1 mol/L) alkalisch machen. Bei Anwesenheit von Magnesium-Ionen entsteht nach ca. 2 Minuten ein hellroter Niederschlag.
- Qualitativer Nachweis von Magnesium, in: Merck (Hrsg.): Die Untersuchung von Wasser. S. 112
- Sabine Venke und Wolfgang Proske: Nachweis von Magnesiumionen in Spinat. In: Friedrich Verlag (Hrsg.): Naturwissenschaften im Unterricht Chemie (Zeitschrift), Heft 120, S. 11 (2010).