Stöchiometrie: Lösungen: Unterschied zwischen den Versionen
Aus BS-Wiki: Wissen teilen
Dg (Diskussion | Beiträge) |
Dg (Diskussion | Beiträge) |
||
| Zeile 1: | Zeile 1: | ||
== Airbag == | == Airbag == | ||
| − | a) Wie viel | + | a) Wie viel [[Natriumazid|Natriumazid (NaN<sub>3</sub>)]] wird benötigt, um einen Fahrer-Airbag mit 60 Liter [[Stickstoff]] zu befüllen? |
#[[Reaktionsgleichung]] formulieren: 2 Fe<sub>2</sub>O<sub>3</sub> + 3 C [[Bild:Pfeil.gif]] 4 Fe + 3 CO<sub>2</sub> | #[[Reaktionsgleichung]] formulieren: 2 Fe<sub>2</sub>O<sub>3</sub> + 3 C [[Bild:Pfeil.gif]] 4 Fe + 3 CO<sub>2</sub> | ||
#[[Molare Masse]]''n'' berechnen: ''M(Fe<sub>2</sub>O<sub>3</sub>)'' = 159,697 g/mol; ''M(Fe)'' = 55,85 g/mol | #[[Molare Masse]]''n'' berechnen: ''M(Fe<sub>2</sub>O<sub>3</sub>)'' = 159,697 g/mol; ''M(Fe)'' = 55,85 g/mol | ||
Version vom 25. Februar 2016, 16:39 Uhr
Airbag
a) Wie viel Natriumazid (NaN3) wird benötigt, um einen Fahrer-Airbag mit 60 Liter Stickstoff zu befüllen?
- Reaktionsgleichung formulieren: 2 Fe2O3 + 3 C
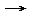 4 Fe + 3 CO2
4 Fe + 3 CO2 - Molare Massen berechnen: M(Fe2O3) = 159,697 g/mol; M(Fe) = 55,85 g/mol
- Verhältnisgleichung unter Berücksichtigung der stöchiometrischen Faktoren gemäß Reaktionsgleichung aufstellen: m(Fe2O3) = 2 · M(Fe2O3) · m(Fe) / 4 · M(Fe)
- Einsetzen: m(Fe2O3) = 159,697 g/mol · 10 t / 2 · 55,85 g/mol
- Ergebnis berechnen: m(Fe2O3) = 14,3 t bzw. 14.297 kg
Roheisenherstellung
a) Wie viel Eisenoxid muss eingesetzt werden, um 10 Tonnen reines Eisen zu gewinnen?
- Reaktionsgleichung formulieren: 2 Fe2O3 + 3 C
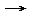 4 Fe + 3 CO2
4 Fe + 3 CO2 - Molare Massen berechnen: M(Fe2O3) = 159,697 g/mol; M(Fe) = 55,85 g/mol
- Verhältnisgleichung unter Berücksichtigung der stöchiometrischen Faktoren gemäß Reaktionsgleichung aufstellen: m(Fe2O3) = 2 · M(Fe2O3) · m(Fe) / 4 · M(Fe)
- Einsetzen: m(Fe2O3) = 159,697 g/mol · 10 t / 2 · 55,85 g/mol
- Ergebnis berechnen: m(Fe2O3) = 14,3 t bzw. 14.297 kg