Indikatoren: Unterschied zwischen den Versionen
Dg (Diskussion | Beiträge) (→Das pH-Meter) |
Dg (Diskussion | Beiträge) (→Das pH-Meter) |
||
| Zeile 13: | Zeile 13: | ||
== Das pH-Meter == | == Das pH-Meter == | ||
| − | Das pH-Meter (Bild 2) dient zur schnellen und genauen Bestimmung von pH-Werten. Durch eine Elektrode erzeugt es eine Spannung, welche vom pH-Wert abhängt. [[PH-Wert-Berechnung|Alternativ ist der pH-Wert auch zu berechnen]], siehe | + | Das pH-Meter (Bild 2) dient zur schnellen und genauen Bestimmung von pH-Werten. Durch eine Elektrode erzeugt es eine Spannung, welche vom pH-Wert abhängt. [[PH-Wert-Berechnung|Alternativ ist der pH-Wert auch zu berechnen]], siehe Übungsaufgabe. |
[[Bild:PH-meter.jpg]] | [[Bild:PH-meter.jpg]] | ||
Version vom 19. Januar 2006, 23:47 Uhr
Inhaltsverzeichnis
Was sind Indikatoren?
Das Wort Indikator leitet sich von dem lat. Wort "indicare" ab, was "anzeigen" bedeutet. In der Chemie ist ein Indikator ein Stoff oder ein Gerät, welches zur Überwachung von einer chemischen Reaktion oder eines chemischen Zustandes dient.
Säure/Base-Indikatoren
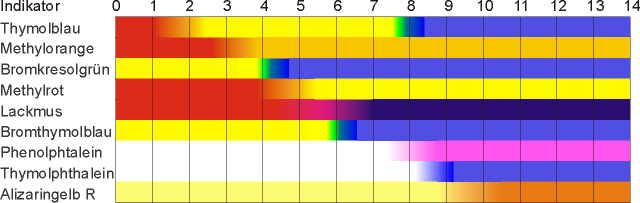
Säure/Base-Indikatoren sind im allgemeinen organische Säuren, welche sich in ihrer Farbe zur korrespondierenden Base unterscheiden. Bsp.: Gibt man zu dem Indikator Methylorange eine (starke) Säure, ist eine rote Färbung erkennbar. Gibt man eine Base hinzu, färbt sich der Indikator gelb (siehe auch Bild 1).
Umschlagsbereiche von Säure/Base-Indikatoren
Die Farbe eines Indikators ergibt sich aus dem Gleichgewicht von Säure zu korrespondierender Base. Ein Farbwechsel ist allerdings erst beim 10-fachen Überschuss einer der Komponenten vollständig auf der pH-Skala sichtbar. Indikatoren können einen bis zwei Umschlagsbereiche (Bild 1) besitzen.
Das pH-Meter
Das pH-Meter (Bild 2) dient zur schnellen und genauen Bestimmung von pH-Werten. Durch eine Elektrode erzeugt es eine Spannung, welche vom pH-Wert abhängt. Alternativ ist der pH-Wert auch zu berechnen, siehe Übungsaufgabe.
Versuch
Damit Sie die Wirkung von Indikatoren besser nachvollziehen können, haben wir hier einen einfachen Versuch für Sie.
Materialien: 2 Behältnisse (möglichst durchsichtig z.B. Glas), 1 Teelöffel, Schwarzer Tee (zubereitet, jedoch nicht zu stark, evtl. mit Wasser verdünnen), Zitronensaft, Spülmittel (nicht pH-Hautneutral!)
Versuchsaufbau: Beide Behältnisse mit schwarzem Tee füllen
Versuch: In ein Behältnis mit Schwarem Tee Zitronensaft und in das andere Spülmittel geben und gut umrühren.
Ergebnis: Der Schwarze Tee, in den der Zitronensaft gegeben wurde, wird heller. Der, in den man Spülmittel gegeben hat, wird dunkler. (kommt man nicht zu diesem Ergebnis war der Tee zu stark, noch mal mit stärker verdünntem Tee ausprobieren)
Übungsaufgabe
-Problemstellung: pH-Wert-Berechnung von Essigsäure (schwache Säure)
-gegeben: c=0,01mol·l-1, pKS=4,65
-gesucht: pH-Wert
-allg. Formel: pH=1/2·(pKS-lg c(HA))
Bsp.:
pH=1/2·(4,65-lg 0,01mol·l-1)
pH=1/2·(4,65+2)
pH=3,325
pH≈3,33
-Lösung: Der pH-Wert von Essigsäure beträgt 3,33.
Power Point Präsentation
In dieser Präsentation ist auch noch ein zweiter Versuch zu finden
Powerpoint-Präsentation zum Thema Indikatoren
Fragen
1. In einer Natriumhydrogencarbonat-Lösung zeigt Phenolphthalein eine blassrosa Färbung. Welcher pH-Wert wird dadurch ungefähr angezeigt?
2. Was passiert mit Thymolblau, wenn man eine Säure mit dem pH-Wert 1 hinzufügt?
Quellen
Bild: Indikatoren: de.wikipedia.org/wiki/Bild:S%C3%A4uren_und_Laugen_-_Farbspektrum_verschiedener_Indikatoren.png;
Bild: pH-Meter: www.mbcoct.com/corning/images/90464.jpg;
Chemie heute Seite 118
Chemie heute - Sekundarbereich II, Schroedel Verlag, ISBN 3-507-10630-2, S. xxx.
Autoren
--Lena
--Janina