Peptidbindung: Unterschied zwischen den Versionen
Joh (Diskussion | Beiträge) (→Struktur der Peptidgruppe) |
Joh (Diskussion | Beiträge) (→Peptide) |
||
| Zeile 17: | Zeile 17: | ||
(von griech.: peptos = verdaulich). Bez. für durch Peptid-Bindungen Säureamid-artig verknüpfte Kondensationsprodukte von Aminosäuren. | (von griech.: peptos = verdaulich). Bez. für durch Peptid-Bindungen Säureamid-artig verknüpfte Kondensationsprodukte von Aminosäuren. | ||
Siehe Artikel [[Aminosäuren]] von Jana und Imke Spö. | Siehe Artikel [[Aminosäuren]] von Jana und Imke Spö. | ||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
==Peptidbinung== | ==Peptidbinung== | ||
Version vom 20. November 2006, 22:05 Uhr
Inhaltsverzeichnis
Proteine
(Eiweiße, Eiweißstoffe, Eiweißkörper). Auf Berzelius zurückgehende u. seit Mulder (1838) gebräuchliche u. von griech.: proteuein = „der Erste sein“ abgeleitete Sammelbez. für natürlich vorkommende Copolymere, die sich in der Regel aus 20 verschiedenen a-Aminosäuren (im folgenden: AS) als Monomeren zusammensetzen. Von den nahe verwandten Polypeptiden werden sie aufgrund ihrer mol. Größe unterschieden, wenn auch nicht immer streng abgegrenzt: Ab etwa 100 Monomer-Einheiten (AS-Resten) spricht man meist von Proteinen. Es ergeben sich MR von 10 000 bis mehrere Millionen. siehe Artikel Proteine von Franci & Kathi
Peptide
(von griech.: peptos = verdaulich). Bez. für durch Peptid-Bindungen Säureamid-artig verknüpfte Kondensationsprodukte von Aminosäuren. Siehe Artikel Aminosäuren von Jana und Imke Spö.
Peptidbinung
Eine Peptidbindung (-NH-CO-) ist eine Bindung zwischen der Carboxylgruppe einer und der Aminogruppe einer zweiten Aminosäure.
Zwei Aminosäuren können (formal) unter Wasserabspaltung zu einem Dipeptid kondensieren.
Im Beispiel reagieren zwei Moleküle der einfachsten Aminosäure Glycin zu einem Dipeptid: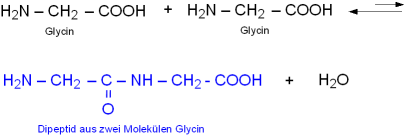
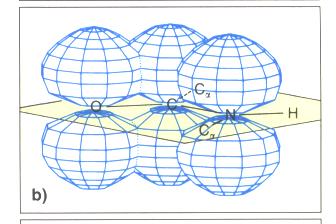
Struktur der Peptidgruppe
- Bestiummung der Bildungslänge in Peptidbindung durch Röntgenstrukturanalyse.
- CN-Bindung ist kürzer als bei Aminen Doppelbindungscharakter
- durch die Delokalisierung der Peptidgruppe ist ein besonders stabil Verbindungsverhältnis erreicht.
-Amid-Gruppe ist planar gebaut das heißt alle am Aufbau der der Verbindung beteiligten Atome liegen auf einer Ebene
- der Diederwinkel liegt daher bei 180° --> Atome können nicht verdreht werden
Aufgabe
Glutathion ist ein Tripeptid mit der Aminosäuresequenz (Glu-Cys-Gly). Es schützt in lebenden Zellen Verbindungen vor Oxidation.Dabei wird Glutathion selbst oxidiert. (m(Glutathion)=307 g x mol-1;M(Oxidationsprodukt)= 612g x mol-1)
a)Geben Sie die Strukturformel des Tripeptids als Zwitterion an, beachten Sie dabei, das Glutaminsäure im Glutathion eine y-Peptidbindung ausbildet
b)Leiten Sie die Strukturformel des Oxidationsproduktes aus Angaben der molaren Masse ab
c) Gebe die Reaktionsgleichung der Oxidation mit Hilfe der Strukturformeln an. Benenne den entstehenden Bindungstyp. Peptidbindung: Antwort
Versuch
Biuret-Reaktion Der Klassische Nachweis von Proteinen geschieht mit der Biuret-Reaktion.
Chemikalien: Eiklar-Lösung(Eiklar+ physiologische Kochsalz-Lösung,diverse Lebensmittel(Fleisch,Nudeln,Kartoffeln,Milch, u.a. Natronlauge 1-7% Geräte: Reagenzglas mit Stopfen,Reagenzglasständer,Reibschale mit Pistill,Tropfpipette,Messpipette 5ml
Durchführung: In das Reagenzglas gibt man etwa 2ml Eiklar-Lösung.Andere Lebensmittel werden in der Reibeschale zerkleinert,mit wenig Wasser aufgeschlämmt und vorsichtig erwärmt, dann werden etwa 2ml der Lösung in das Reagenzglas dekantiert.Man gibt nun 2 ml Natronlauge hinzu, verschließt das Glas mit dem Stopfen und schüttelt gut durch jetzt werden 3Tropfen der Kupfersulfat-Lösung zugefügt.
Ergebnis: Bei Anwesenheit von Protein entsteht ein gelber Fleck
Quellen
Chemie heute Seite 375 Kapitel 19.8,Römpp Lexikon Chemie – Version 2.0, Stuttgart/New York: Georg Thieme Verlag 1999 Versuch aus Unterricht Cemie BAnd 11 : lebnsmittel-Nährstoffe Heinz Schmidkunz, Karin Schlagheck Aulis verlag Deubner & Co KG
