Oxidationszahl: Lösungen: Unterschied zwischen den Versionen
Rike (Diskussion | Beiträge) (→Aufgabe 4) |
Lena (Diskussion | Beiträge) (→Aufgabe 2) |
||
| Zeile 26: | Zeile 26: | ||
<br> | <br> | ||
{{oxi| III|Fe<sup>3+</sup>}} | {{oxi| III|Fe<sup>3+</sup>}} | ||
| + | |||
{{oxi| I -I|NaH}} | {{oxi| I -I|NaH}} | ||
| + | |||
{{oxi| I -II|H<sub>3</sub>O<sup>+</sup>}} | {{oxi| I -II|H<sub>3</sub>O<sup>+</sup>}} | ||
| + | |||
{{oxi|I VII -II|KMnO<sub>4</sub>}} | {{oxi|I VII -II|KMnO<sub>4</sub>}} | ||
| + | |||
{{oxi| VI -II|CrO<sub>4</sub><sup>2-</sup>}} | {{oxi| VI -II|CrO<sub>4</sub><sup>2-</sup>}} | ||
| + | |||
{{oxi|I V -II|KClO<sub>3</sub>}} | {{oxi|I V -II|KClO<sub>3</sub>}} | ||
| + | |||
{{oxi| II -II|S<sub>2</sub>O<sub>3</sub><sup>2-</sup>}} | {{oxi| II -II|S<sub>2</sub>O<sub>3</sub><sup>2-</sup>}} | ||
Version vom 14. März 2007, 23:56 Uhr
Ermittle die Oxidationszahlen der folgenden Atome in folgenden Verbindungen und Ionen!
Inhaltsverzeichnis
Aufgabe 1
Cl2, H2S, H2O2, CO2, ClO2, HNO3, CH4, SiH4, NH3, P4O10
Lösungen:
0
Cl2
I -II
H2S
I -I
H2O2
IV -II
CO2
IV -II
ClO2
I V -II
HNO3
-IV I
CH4
-IV I
SiH4
-III I
NH3
V -II
P4O10
Aufgabe 2
Fe3+, NaH, H3O+, KMnO4, CrO42-, Cr2O72-, KClO3, S2O32-
Lösungen:
III
Fe3+
I -I
NaH
I -II
H3O+
I VII -II
KMnO4
VI -II
CrO42-
I V -II
KClO3
II -II
S2O32-
Aufgabe 3
Methanol, Formaldehyd, Ameisensäure, Benzol, Propan, Glucose, Propanon, Chloroform
Lösungen:
Methanol
-II I -II I
CH3OH
Formaldehyd
I -I
CH2O
Ameisensäure
II I -II
CH2O2
Benzol
-I I
C6H6
Propan
-III I -II I -III I
CH3-CH2-CH3
Glucose
| [[Oxidationszahl|]]
|
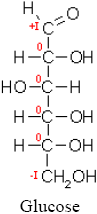
|
Propanon
|
|
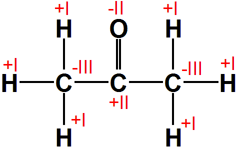
|
Chloroform
II I -I
CHCl3
Aufgabe 4
Ermittle die Oxidationszahlen für die folgenden Lebensvorgänge bzw. Stoffwechselreaktionen. Formuliere zunächst die Reaktionsgleichungen:
- a) Atmung als Oxidation organischer Stoffe am Beispiel Glucose: C6H12O6 + 6O2
 6CO2 + 6 H2O
6CO2 + 6 H2O
Lösung:
0 I -II
C6H12O6
+ 0
6O2
![]() IV -II
IV -II
6CO2
+ I -II
6H2O
- b) „Schwefelatmung“ der Archae-Bakterien, die Glucose mit Schwefel und Wasser zu Schwefelwasserstoff und Kohlendioxid umsetzen. Der Schwefel wird bei dieser Reaktion reduziert: C6H12O6 + 12S + 6H2O
 6CO2 + 12H2S
6CO2 + 12H2S
Lösung:
0 I -II
C6H12O6
+ 0
12S
+ I -II
6H2O
![]() IV -II
IV -II
6CO2
+ I -II
12H2S